 大赌局
大赌局读书摘要《生物医学研究的统计方法》知识小结—方积乾
生物医学研究的统计方法本书是生物医学研究生使用的经典统计教材,内容易懂经典,无需多少数学基础都能看懂。本书每个章节后面都有知识小结,现汇总以供大家学习。--------------------------------------------------------------------------------------(1) 统计学是关于设计与数据的学问,是从特定环境中获取数据并从数据中提取信息、知识的一门科学与艺术,包括研究设计、数据搜集、数据整理、数据分析和结果报告等步骤。(2) 根据结果(效应)变量的类型、分析目的和资料具备的前提条件等,选择不同的统计学分析方法。变量可分为定量变量与定性变量两大类。定性变量也叫分类变量,根据类别之间有无大小顺序,可将定性变量分为有序(等级)分类变量和无序(名义)分类变量。定量变量有离散和连续之分,定性变量只能是离散变量。(3) 统计工作贯穿于医学研究的全过程,包括研究设计、数据搜集、数据整理、数据分析和结果报告等,切不可将统计工作仅仅局限于“数据分析”。(4) 根据一定研究目的搜集到的资料蕴涵着丰富的信息,统计描述的目的就是用恰当的手段(编制统计表、绘制统计图或计算统计指标)概括地呈现出主要信息。(5) 明确资料的类型,采用不同指标进行统计描述。1)定量资料;描述平均水平可以依据分布特点选用算术均数、几何均数、中位数、众数或调和均数,描述变异程度可以选用全距、标准差、方差、四分位数间距或变异系数(表1)表1 定量资料统计描述常用的统计指标及其适用场合表2 定性资料统计描述常用的统计指标及其适用场合表3 常用统计图的适用资料及实施方法(6) 正态分布是一种重要的连续型分布。若连续随机变量X的概率密度函数为则称X服从总体均数为μ,总体标准差为σ,的正态分布,记作X~N(μ,σ2)。正态分布N(μ,σ2)关于x=μ对称。μ决定正态曲线在横轴上的位置,μ增大,则曲线沿X轴向右移动;反之,μ减小,曲线沿X轴向左移动。σ决定曲线的形状,当μ固定时,σ愈大,表示数据愈分散,曲线愈“矮胖”; σ愈小,数据集中在μ附近,曲线愈“瘦高”。服从正态分布N(μ,σ2)的随机变量在某个区间内取值的概率即为其概率密度曲线下的面积。X取值落在区间μ士1.64σ, μ士1.96σ, μ士2.58σ的概率分别是90%,95,99%,或者说在理论上μ士1.64σ, μ士1.96σ, μ士2.58σ。三个范围内的观察数分别占总观察数的90%、95%、99%。总体均数为σ,总体标准差为1的正态分布称为标准正态分布,记作N(0,1)。服从任意正态分布N(μ,σ2),的变量X都可以通过标准正态变换转化为标准正态分布,从而使正态分布的概率计算问题转化为标准正态分布,进而利用标准正态分布表解决。(7) 二项分布是一种重要的离散型分布,用于描述两分类资料(结果只能出现两种情况)的n次独立重复试验中发生某种阳性结果为X次的概率分布。若随机变量X的概率函数为则称X服从参数为n、π的二项分布,记为X~B(n,π)二项分布B(n,π)的总体均数μ=nπ,总体标准差。(8) Poisson分布也是一种重要的离散型分布,用于描述单位时间或空间内某稀有事件发生数的概率分布。若随机变量X的概率函数为则称X服从参数为产的Poisson分布,记为X~Π(μ)Poisson分布Π(μ)的总体均数和总体方差相等,即μ=σ2。(9) 从同一总体中,随机抽取相同含量的样本,由重复抽取的每一份样本均可计算获得一个样本统计量,样本统计量的分布就是抽样分布。(10) 样本统计量所对应的标准差统计学上习惯地称为标准误,标准误反映抽样误差的大小,即反映总体特征被估计的精确程度。(11) 标准误与样本含量的平方根成反比,样本含量越大,抽样误差越小。(12) 统计推断是根据抽样分布规律,采用样本统计量对相应总体参数所作的非确定性的推断,主要包括参数估计和假设检验两种。参数估计有点估计和区间估计两种。区间估计是按事先给定的置信度((1-α),估计可能包含未知总体参数的一个范围,该范围称为总体参数的((1-α)置信区间。(13) 假设检验是依据样本提供的有限信息、对总体作推断的逻辑推断过程,是对研究总体的两种对立的假设作出选择。假设检验的步骤为:建立假设→计算统计量→确定P值→作出推断结论。假设检验的基本逻辑是根据小概率的思想,认为“小概率事件在一次抽样中不太可能出现”。假设检验存在Ⅰ类错误和Ⅱ类错误。根据假设检验的推断结果下结论时不能绝对化,并要注意结合专业知识。(14)两样本定量资料假设检验的流程对于完全随机设计的两样本定量资料的假设检验,是采用t检验还是秩和检验要看资料是否符合各自的条件。t检验要求资料满足正态性和方差齐性。对于配对设计资料的假设检验,首先看差值是否符合正态分布,如果差值满足正态分布,可以采用配对t检验,否则,采用变量变换使之满足正态性要求或采用配对资料的符号秩和检验。(15) 三个或三个以上均数间的比较可以采用方差分析,以检验多个平均值是否来自相同总体,其实也可用于两个均数间的双侧假设检验,此时结果与t检验完全等价。本章介绍了方差分析中最简单的单因素方差分析,可以用于完全随机设计的实验性研究和多总体随机抽样的观察性研究。(16)方差分析的基本思想即将处理间平均变异与误差平均变异比较。就完全随机设计的资料而言,将全部观测值总的离均差平方和及其自由度分解为组间变异和组内变异两个部分,两者分别由处理因素和随机误差的作用加以解释。通过比较不同变异来源的均方,借助F分布作出统计推断,从而推论处理因素对实验结果有无影响。(17)多组定量资料比较的思路首先进行方差齐性及各样本的正态性检验。若方差齐性,且各样本均服从正态分布,选单因素方差分析。对于明显偏离正态性和方差齐性条件的资料,通常有两种处理方式:一是通过某种形式的数据变换以改善其假定条件,二是改用非参数统计方法Kruskal-Wallis秩和检验。若方差分析或秩和检验结果有统计学意义,则需选择合适的方法(如Bonferonni, LSD法等)进行两两比较。(18) 对于定性资料,我们经常将它整理成列联表的形式。(19) 最简单的列联表是2X2表,即通常所说的四格表。按照设计类型,将资料整理成相应的四格表格式,统计分析时选用相应的统计分析方法。(20)在选用χ2检验时,一定要考虑其对总例数和理论频数的要求。(21) 当多个独立样本频率或频率分布比较的χ2检验,结论为拒绝检验假设时,只能认为各总体频率或频率分布之间不全相同,若想了解其差别的具体情况,需要进行多个样本频率或频率分布的两两比较。(22) 列联表资料统计分析的χ2检验不是万能的。例如,对于有序分类资料,最好选用秩和检验。对于高维列联表资料,相应地有对数线性模型和logistic回归模型等。(23) 相关是测量变量间的相互关联或联系的指标。相关研究的两个变量其关系是平等的,均为随机变量。(24) 在分析相关时必须先作散点图,以核实其是否具有线性关系及是否有异常点或应分层等情况,推荐在报告结果时也提供散点图并说明散点图的特征。(25) 两连续变量间的相关分析方法主要有Pearson积矩相关和Spearman秩相关。前者要求两个变量皆为随机变量,呈双变量正态分布,样本间独立,变量间有线性趋势;当资料不满足正态分布条件或为等级资料时,采用Spearman秩相关方法。两者的计算思想是一致的,但秩相关不使用原始数据而使用秩次进行计算。计算出相关系数后,还应进行假设检验,甚至计算相关系数的置信区间。(26) 分类资料的关联分析可区分为二分类和多分类的情形,检验都采用χ2检验。分类资料的关联性检验应与率的比较检验相区别。若检验结果拒绝两变量独立的假设,则可计算关联系数。(27) 相关和关联是两变量间相互关联或联系数量上的关系,不能据此推论两变量有生物学的联系,或有因果关系。相关有可能只是伴随关系。(28) 简单线性回归分析的基本步骤①绘制散点图,考察两变量是否有线性趋势及可疑的异常点;②估计回归系数与截距;③对总体回归系数或回归方程进行假设检验;④列出回归方程,绘制回归直线;⑤统计应用。(29) 简单线性回归是指只包含一个自变量,且呈线性变化趋势的线性回归模型,用于描述因变量的总体均数与自变量之间的线性关系,亦称两变量间的依存变化关系。在实际应用中,两变量间的关系应有实际意义,不要把毫无关联的两种现象作回归分析。(30) 简单线性回归方程包括截距与回归系数两个参数,通常采用最小二乘估计。(31) 通过对Y的总变异分解有助于理解简单线性回归分析的基本思想,即Y的离均差平方和(SS总)分解为回归平方和(SS回归)与残差平方和(SS残差)。(32) 线性回归分析的主要用途为预测与控制。在实际应用中,要注意回归方程避免外延,即简单线性回归方程的适用范围一般以自变量的取值范围为限,除非有充分理由证明在此范围外仍然有效,否则预测或控制不宜超出此限。(33) 当两变量变化趋势为非线性时,可考虑拟合非线性回归方程,常用的曲线类型包括指数曲线、多项式曲线、双曲线和logistic曲线等。(34) 多重线性回归是简单线性回归的拓展,用于研究一个反应变量与多个自变量之间的线性依存关系。多重线性回归在医学研究中常常用于筛选危险因素、控制混杂因素、分析交互效应、预测与控制等。(35) 多重线性回归分析的假定条件是线性、独立、正态及方差齐性。常常采用残差分析考察资料是否满足这四个前提条件。如果不满足前提条件,可以尝试对变量进行变换,引入交互作用项或者更换回归方程。(36) 多重线性回归分析中常常采用最小二乘法估计模型参数。多重线性回归分析中偏回归系数的含义是当其他自变量的取值固定时,自变量每改变一个单位,反应变量平均改变的单位数。标准化偏回归系数常用于比较自变量对反应变量的贡献大小。确定系数和调整的确定系数常用于评价模型拟合效果的好坏。对整个回归模型的假设检验一般采用方差分析,对各总体偏回归系数是否为零的假设检验常采用t检验。(37) 多重线性回归分析中筛选自变量的方法有前进法、后退法、逐步回归法和最优子集法等。用于筛选自变量的指标有残差平方和、残差均方、确定系数、调整的确定系数、Cp,统计量等。(38) 当自变量间存在较强的相关时,多重线性回归模型会出现多重共线性现象,使得模型参数估计值不稳定或不易解释。(39) 多重回归分析的一般步骤:①单因素方程分析;②逐步筛选变量,建立多因素方程;③综合单因素和多因素模型的结果,当两者矛盾时,结合专业知识分析原因。另外,要注意因素之间是否存在交互作用。(40) 实验设计主要有以下三点作用:合理安排各种实验因素和区组因素,以提高实验效率;控制和减少实验误差,以提高研究质量;通过较少的实验次数获取尽可能丰富的信息,以便由样本信息去准确地推论总体的规律性。(41) 为了保证实验的可靠性和可重复性,在实验设计中所用的随机化方法、随机数及产生随机数的程序、种子数等均应有记录。(42) 单因素设计和统计分析都比较简单,但实验效率较低,只能考察一个因素对观测结果的影响情况。各组实验单位数可以相等或不等,但不应相差悬殊。当两处理组比较时常用t检验或秩和检验,多个处理组比较时常采用相应设计定量资料的方差分析或秩和检验。(43) 配对设计能有效地降低来自个体差异对观测结果的影响,从而减小实验误差,提高实验效率。但采用配对设计时,要防止偏性,尽可能保持每对受试对象的均衡和齐同。配对的条件应当是本实验研究中对观测结果有重要影响的所有非实验因素的组合结果,而绝对不能随便选取一个非实验因素作为配对条件,那样只能是在表面上缩小了实验误差,其结果是容易增大结论犯假阳性错误的概率。(44) 随机区组设计是在单因素设计的基础上,多考虑一个区组因素。这个区组因素的不同水平反映了受试对象在重要的条件上的差异,若不将其排除,必然会影响对实验因素各水平之间差别大小的正确评价,即造成了两个因素效应的混杂。(45) 交叉设计平衡了实验顺序对结果的影响,并且能将处理间的差别与阶段间的差别有效区分开来,每个个体接受两种处理,节约了样本含量;但本设计不适用于具有自愈倾向或病程短的研究,每个个体在接受两种处理之间应有足够长的洗脱期。(46) 析因设计是一种比较常见的多因素实验设计。在实验研究中应用得比较频繁。一般来说,如果在实验设计中涉及的实验因素不超过5个,在专业上有必要考察因素之间的各级交互作用,每个因素的水平数比较少且每次实验花费较少、费时较短时,可以考虑使用析因设计。(47) 重复测量设计的主要优点是可以减少样本含量,能够有效地考察指标随时间推移的动态变化趋势。重复测量是在同一受试者身上进行的,因此,在不同时间点上观测指标的取值之间一般是不独立的,后一次测量结果可能受到前面各次测量结果的影响。因此,对同一个体在不同时间点上的测量值之间就可能存在相关关系,就需要用特殊的统计分析方法进行分析。(48) 调查研究是一种没有采取任何干预措施的研究工作,它主要是对客观存在的现象进行询问和观察,故调查研究又称为观察性研究,它被广泛地应用于生物医学、社会学及教育学等多个领域。(49) 调查研究的目的主要有描述、分析、检验假设、评价、预测。(50) 调查研究的步骤主要分三步:首先是设计阶段或准备阶段,包括发现和提出问题、复习文献、立题、调查设计;其次是现场调查工作阶段,包括预调查、收集数据资料;最后是资料整理、表达及分析阶段,包括整理分析资料、解释和交流研究结果。(51) 调查设计是对整个调查研究作出科学完整的计划,其目的是以较少的人力、物力和财力获取较丰富而可靠的资料,同时将各种误差降到最低限度,它主要包括:确定调查目的与指标,确定调查对象和观察单位,确定调查方法、调查设计类型、抽样方法和资料收集方式,设计调查表,估计样本含量以及调查的组织实施与质量控制。调查设计是调查研究中的第一道工序和重要环节,它的好坏直接影响到研究工作的质量。(52)调查表是调查工作中收集资料的最主要的测量工具,它主要是由一系列与研究目标有关的问题组成的问卷。调查表的构成有标题、调查项目(背景资料、研究项目变量、核查项目)、编码和填表说明。(53) 问卷调查表的评价方法主要有效度评价和信度评价,其中效度评价又包括表面效度、内容效度和结构效度,信度评价包括重测信度、内部信度(克朗巴赫a系数和分半信度)和测评者之间信度。(54) 常用的调查研究方法有:横断面调查,它又可分为普查和抽样调查(如单纯随机抽样、系统随机抽样、分层随机抽样、整群抽样和多阶段抽样);病例一对照研究;队列研究。(55) 常用的调查设计类型有:横断面调查研究设计、病例对照研究(回顾性调查)设计和队列研究(前瞻性调查)设计。(56) 调查研究中应注意的问题有:明确调查目的,制定周密的调查设计及问卷,考虑并规范调查所涉及的伦理道德问题,选择适当的调查方法、调查设计类型和抽样方法,重视预调查,加强调查研究全过程的质量控制。(57) 分析数值型变量的方法很多,读者应先确定研究的设计类型,据此选择合适的分析方法中常见的错误为:误将随机区组设计资料和析因设计资料用单因素方差分析或t检验方法分析分析过程随机区组设计资料(58) 析因设计资料很容易与完全随机设计资料混淆,读者应仔细辨别。与单因素方差分析相比,随机区组设计资料的方差分析可根据设计进一步分解变异,控制其他非处理因素对实验效应的影响。(59) 随机区组设计资料的方差分析不能分析因素间的交互效应,而析因设计资料则既可以分析因素的主效应,也可以分析其单独效应和交互效应。(60) 分析随机区组设计资料和析因设计资料时应注意资料是否满足方差分析的条件,若资料不满足方差分析的条件,可经变量变换使之满足条件,然后再用方差分析的方法分析之,或用非参数检验的方法分析之。(61) 当球形检验的P小于0.1时,重复测量的各个时间观察点资料之间的方差齐性或不同组别的方差齐性不满足,只能用SPSS的重复测量专用模块,并且选用校正自由度的Greenhouse-Geisser检验统计量及其对应的P值作统计推断。(62) 在重复测量资料的统计分析中,当存在交互作用时,可以推断对于不同重复测量时间点的两组所对应的两个总体均数之差是不全相同的,但进一步作两两比较的统计分析比较复杂,建议请专业的统计工作者帮助进行统计分析。(63) 如果在重复测量资料的统计分析中,交互作用项没有统计学意义,可以在方差分析中仅引入主效应项,可以增大检验效能,并且还可以使各个时间点的两两比较简单化,但即使没有交互作用时,对于多组情况下的组间两两比较仍要谨慎。所以,许多研究者当统计结果显示存在交互作用时,一般采用作图作趋势分析,得到大致的统计推断。(64) 在两阶段的交叉设计研究中,不存在延滞效应与处理效应的交互作用,但在多阶段的交叉设计研究中(如三阶段交叉设计研究等),要考虑延滞效应与处理效应的交互作用,否则可能导致效应估计偏倚。(65)Logistic回归适合因变量为分类变量的研究问题,自变量可以是定量变量、有序或无序分类变量。对于定量变量,如果与因变量logit π呈线性关系,以定量变量形式引入方程分析最佳,否则,应离散化并以哑变量形式引入方程分析;有序多分类自变量,可以先以哑变量形式进行分析,如果相邻等级间优势比近似恒定常数,则可对有序分类变量适当赋值,以离散型定量变量引入方程分析;对无序多分类变量,必须以哑变量形式引入方程,并且在变量筛选中整体进/出方程。(66) 按照回顾性病例对照资料建立的logistic回归方程以及条件logistic回归方程,因不能估计事件概率,或因变量预测值不是概率值,不宜应用Hosmer-Lemeshow检验判断方程拟合效果。(67) 似然比检验是logistic回归分析中非常有用的一种检验方法,主要用途有三:①用于回归方程整体拟合优度检验:通过与常数项方程比较,以判断所建立回归方程有无统计学意义,似然比检验统计量的自由度等于回归方程中自变量的个数-1;②用于检验单个变量回归系数βi是否等于0:在已有的回归方程中剔除某自变量Xi,并据此计算相应似然比检验统计量,判断总体回归系数是否为0,似然比检验统计量自由度等于1;③用于回归方程优选:对于两个不同的回归方程,如果一个方程所有自变量包含在另一个方程中,这时可以用似然比检验,以判断何者拟合效果更优,其似然比检验统计量的自由度等于两个方程自变量个数的差值。似然比检验特别适用于无序分类或按无序分类处理的自变量的logstic回归方程。如果两个比较的方程自变量没有嵌套关系,自然就不能使用该方法。(68) 极大似然估计要求个体的结局事件发生与否独立、同分布,所以,对于传染性较强的疾病,不能采用logistic回归方程研究其发病与否的危险因素,或是用于发病概率的预测。——以上资料来源:方积乾《生物医学研究的统计方法》,如有侵权,请联系作者及时删除
 不亦远乎
不亦远乎读书摘要《生物医学研究的统计方法》常见疑问—方积乾
生物医学研究的统计方法本书是生物医学研究生使用的经典统计教材,内容易懂经典,无需多少数学基础都能看懂。本书每个章节后面都有常见疑问,现汇总以供大家学习。--------------------------------------------------------------------------------------(1)如何确定研究总体与样本?总体的定义告诉了我们,总体是根据研究目的确定的同质研究对象的全体,也就是说确定什么样的总体与下列因素有关:①研究的目的是什么;②研究对象是否同质(即使非处理因素尽可能相同);③是否为研究对象的全体。样本是从总体中抽取的部分研究对象,确定样本应该注意:①样本是总体中的部分研究个体;②样本是能代表总体的样本。相对样本而言,总体应该是“无限总体”或相对的“无限总体”(比如,在样本含量足够的前提下,样本个体数小于总体个体数的500),这是统计学推断的理论基础;如果总体不大,为“有限总体”,则数据分析的主要方法是统计描述;如要进行统计推断,则应对有关指标进行校正。(2)何为连续变量与离散变量?可以在某一区间取任何值的变量就是连续变量,当测量精确度很高时,理论上数据之间无“缝隙”。数据之间存在“缝隙”的变量就是离散变量,如家庭人口数、脉搏跳动次数(次/min)、红细胞计数等,离散变量只能取有限的几个值。定量变量之中,有的属于连续变量,有的属于离散变量;但定性变量只能是离散变量。(3)不同的编码方式,所得结论相同吗?以上提到可将“文化程度”中的文盲、小学、中学、大学(假定为有序变量)及以上分别编码为1,2.3,4,或按读书年数编码为0,6,12,16。无论哪种编码,所得统计学分析的结论(如假设检验所得概率值)应该是一致的,但获得的某些统计量(如回归系数、优势比等)有可能不相同。(4)用恰当指标对定量资料进行统计描述,需要了解变量的分布形式。在实际工作中,是怎样明确变量的分布形式的?变量的分布形式,常可以通过查阅文献得到。例如,文献报道中学生的体重、肺活量服从对称分布,其发硒含量则为正偏峰分布,那么,我们就可以沿用文献的做法。特别当参考文献中的研究是基于大样本时,一般认为变量的分布形式可以直接参照。如果在相关文献中未查到某医学指标的分布规律,而该指标又是我们感兴趣的变量,那么就可以在大样本基础上,借助SPSS等统计分析软件对资料分布形式作统计检验。(5)呈现事物的发展变化速度时,为什么要用半对数线图,而不能用普通线图?在用普通线图表示事物随时间变化而变动的情形时,线条纵向波动的位置仅反映了被研究指标在相应时间点上取值的大小。例如指标取值发生“10→100→1000”的变化时,给读者的提示是,第一阶段增加幅度为90,第二阶段增加幅度为900,第二阶段的增加幅度大于第一阶段。但是,有时研究者欲传达事物演变的变化倍数,例如前述指标在第一阶段发生了“增大到原来的10倍”的变化,而第二阶段也发生了“增大到原来的10倍”的变化,两个阶段变化的倍数相同。普通线图可以直观反映变化的“增量”,却不能描述变化的“倍数”。这时需借助半对数线图,将纵轴的尺度进行对数变换,使得“10→100→1000”的变化成为“1→2→3”,两个阶段的变化幅度均为1,准确地传达了“变化的倍数均为10”这一信息。(6)如何判定一组数据是否符合正态分布?判定一组数据是否符合正态分布,通常有如下几种方法:①根据文献报道。例如,文献报道中学生的体重、肺活量服从正态分布,那么我们可以沿用文献的做法。②根据经验或专业知识判断。例如,根据专业知识,同性别健康成人的红细胞数、血红蛋白含量、脉搏数等都近似服从正态分布,而正常成人的血铅含量近似对数正态分布,经对数转换后应近似服从正态分布。③可以借助统计软件对资料作正态性检验或拟合优度检验。(7)对称分布在“X士1.96S”的范围内,也包括95%的观察值吗?不一定。“均数士1.96标准差”范围内包含95%的变量值是正态分布的分布规律,不是对称分布的分布规律。对称分布不一定是正态分布。(8)如何判定一组资料是否符合Poisson分布?Poisson分布是离散型分布,变量的取值为非负整数,它是描述单位时间(面积、空间)内某罕见事件发生数的概率分布。实际应用中,如果某罕见事件的发生数满足Poisson分布的应用条件,如水中细菌数、单位空间中的粉尘数、单位时间内放射性物质的脉冲数等,都可认为服从Poisson分布。另外,还可以对资料进行Poisson分布的拟合优度检验。(9)何谓置信区间的准确度与精确度置信区间有准确度(accuracy)精确度(precision)两个要素。准确度由置信度(1-α)的大小确定,即由“此区间包含总体参数”这句话可信程度(1-α)的大小来反映,从准确度的角度看,置信度愈接近于1愈好,如置信度99%比95%好;精确度是置信区间宽度的一半,意指置信区间的两端点值离样本统量的距离。从精确度的角度.看,置信区间宽度愈窄愈好。在抽样误差确定的情况下,两者是相互矛后的。若提高了置信度.即α减小。则检验统计量界值增大,置信区间变宽. 从而导致精确度下降;反之,降低置信度,即降低准确度,可适当增加置信区间的精确度。为了同时兼顾置信区间的准确度与精确度,可适当增加样本含量;在置信度确定的情况下,增加样本含量可降低抽样误差,从而缩小置信区间范围,提高参数估计的精确度。(10)置信区间与参考值范围有什么区别?总体均数的置信区间与个体值的参考值范围无论在含义、用途还是计算上均不相同。实际应用时,不能将两者混淆,详见表1表1,置信区间与参考值范围的区别(11)标准差与标准误有什么区别与联系?标准差反映个体观察值围绕均数的散布程度,即反映个体值彼此之间的差异。标准误反映样本统计量(如样本均数)围绕总体参数(如总体均数)散布的程度。根据公式,标准误小于标准差;样本含量越大,标准误越小;但标准差不随样本含量的改变而有明显方向性改变,随着样本含量的增大,标准差有可能增加,也有可能减少。如果需要反映个体的变异程度大小,应采用标准差;如果需要反映由样本统计量估计总体参数的精确程度,应采用标准误或95%置信区间。其区别与联系可小结为表2。表2 标准差与标准误的区别与联系(12) 如果样本来自有限总体,如何作统计推断?统计学推断建立在无限总体的基础之上,如果样本所来自的总体为有限总体(如样本含量n大于5%倍的总体含量N),则前面的标准误计算公式应作适当修改,如样本均数的标准误计算公式应改为样本均数的标准误计算公式样本频率的标准误计算公式应改为样本频率的标准误计算公式其中N为总体中个体的含量,(N-n)/(N-1)称为有限总体校正因子。当样本含量n接近有限总体含量N时,(N-n)l(N-1)接近于0,相应的标准误也接近于0。在绝大多数情况下,目标总体是有限总体,如果总体含量N相对样本含量n很大,此时有限总体校正因子十分接近于1,因此通常情况下可忽略此项。仅当样本含量n大于5%倍的总体含量N情况下,才采用上述公式进行计算。(13) 假设检验中α与P有何不同?α为决策者事先规定的“小概率值”(各种科研杂志习惯上采用0.05或0.01)。在零假设成立的情况下,如果检验统计量取当前值以及取值更不利于H0的概率小于或等于α,则可以认为:在零假设成立的情况下,不大可能在某一次抽样研究中出现当前的事件;但当前的事件居然发生了,我们不禁怀疑零假设是否真的成立,从而拒绝H0推断H1成立。所谓P值是指在H0成立的前提下,出现目前样本数据对应的统计量(如Z、t、F值等)数值乃至比它更极端数值的概率。P值也是一个随机变量,即不同的样本可得到不同的P值。(14)通过假设检验得到P>α.能否说明接受H0时犯错误的可能性很小?不能,因为假设检验时,只是确定犯I类错误的概率a,可以按小概率事件拒绝H0,而不知道犯Ⅱ类错误的概率β,所以不能说明接受H0时犯错误的可能性很小(15)通过假设检验得到P值很小,能否说明比较的总体均数相差很大?所谓P值,是指在H0成立的前提下,出现目前样本数据对应的统计量(如Z、t、F值等)数值乃至比它更极端数值的概率。它不但与均数实际值的差距有关,还与抽样误差的大小有关,所以不能单从P值的大小判断总体均数差距的大小。(16)进行两样本均数比较的t检验时,假设检验结果P值越小,则说明两个总体均数相差越大吗?假设检验中,P是指H0成立时出现目前样本情形的概率最多是多大,P值越小,说明如果H0为真,则“不大可能”出现目前的情况,即有理由怀疑H0为真的无效假设,因而拒绝H0,接受H1,即两总体均数间存在着差值。所以,P值越小越有理由认为两个总体间存在着相差,但并不能反映两个总体均数相差的数值大小。(17)单侧检验较双侧检验更易检验出差别,是否应在假设检验中尽量选用单侧检验?当自由度和检验水准一定时,单侧界值小于双侧界值,所以更容易得出差异性的结论,但并不能因此就选用单侧检验。单双侧的选择要结合专业知识:如果研究者关心的是甲乙两组所属总体均数(或者总体率)有无差别,即甲可能高于乙,乙也有可能高于甲时,一般选双侧;若根据专业知识,甲不会低于乙时,或者研究者仅关心其中一种可能时,可选用单侧。一般来讲,双侧检验较为稳妥。(18)既然秩和检验对资料没有严格的要求,是否在进行两组间均数比较时可直接采用秩和检验?这样做不能认为是错的,但不是最好的分析策略。秩和检验对资料没有严格的要求,但满足正态分布条件时其检验功效比t检验的检验功效低一些,所以通常只用来对偏峰分布资料进行假设检验。(19) t检验能否用于多组间均数的比较?t检验主要用于两组间均数的比较,多组间均数的比较若采用t检验,会增大犯I类错误的概率。所以,多组间均数进行比较时应首先考虑方差分析及SNK,LSD等多个样本均数的两两比较技术(详见方差分析)。(20)如何理解假设检验中的大样本和小样本?为什么样本量较大时不必进行正态性检验?在假设检验中,大样本和小样本只是相对于资料的偏峰程度而言的,偏峰程度越大,要求样本量就越大,但一般情况下,当样本量大于50时,可以理解为样本量较大。此时,即便原始变量X有些偏离正态,其样本均数也会近似正态分布。因此,对大样本资料可以不必进行正态性检验。(21)在成组t检验中,当P<0.05并且时,为什么就能推断?在成组t检验中,当P<0. 05并且,则可以证明的95置信区间的下限大于0,由此在95%置信度的前提下,推断;同理,当P<0.05并且时,则可以证明:的95%置信区间的上限小于0。,由此在95%置信度的前提下,推断。(22)为什么不宜直接对多组定量资料进行方差分析?进行方差分析的数据应满足两个前提:①各样本是相互独立的随机样本,均服从正态分布;②各样本的总体方差相等,即方差齐性(homogeneity of variance)。因此,对多组定量资料进行方差分析首先要进行方差齐性及各样本的正态性检验,符合方差分析的条件再行方差分析及必要时进一步的两两比较。否则,若不满足方差分析条件,则需作数据变换,使其满足方差分析的条件,或选Kruskal-Wallis秩和检验。(23)若三个样本均数的比较经ANOVA分析有统计学意义,在多重比较中出现了“不拒绝μ1≠μ2,也不拒绝μ1≠μ3,但拒绝μ2=μ3”的结果,该结果应如何解释?为什么?按假设检验的基本原理,该结果可解释为:有理由认为μ2≠μ3,但还没理由认为μ1≠μ2及μ1≠μ3。因为统计结论在一定概率意义下成立,不能按确定性数学方式递推。该结果既不能解释为:μ1介于μ2和μ3之间;也不能递推为:μ2=μ1,同时μ1=μ3,那么μ2=μ3。(24)是否一定要经ANOVA发现有统计学意义后,再作均数间的两两比较?一般地说,经ANOVA发现有统计学意义后,再作均数间的两两比较,但不是绝对的。实际上,这种ANOVA发现有统计学意义后,再作均数间的两两比较属于事后未计划的比较。均数间两两比较的方法很多,有十余种之多。并且也不很成熟。有些统计学专家提出某些多重比较可不依赖方差分析的结果。另外,在分析资料时有时会出现ANOVA有统计学意义而两两比较均无统计学意义,或ANOVA无统计学意义而两两比较某些均数间有统计学意义的现象,这两种现象往往发生于算得的P值在规定的检验水准α附近,下结论时需特别谨慎。(25)多重比较的方法很多,可否各种方法都用一用,哪个方法给出的P值好,就报告哪个方法的结果?多重比较的方法很多,多重比较时甚至会出现某些方法间(如Bonferroni法与LSD法)统计结果不一致现象,这实际上涉及多样本均数两两比较方法选择的问题。要根据研究的目的选择两两比较的方法。当在设计阶段就根据研究目的或专业知识而计划好某些均数间的两两比较、用于探索性研究时,可选用LSD法,即选用LSD法结果。LSD法灵敏度比较高,但Ⅰ类错误可能会增大,适用于组数g较小且仅对某些特定的组间比较感兴趣时; 当在研究设计阶段未预先考虑或预料到,经假设检验得出多个均数不等的提示后,才决定多个均数的两两比较时可选用Bonferroni。Bonferroni法比较简单,广泛应用于不同场合的两两比较,但结论比较保守,可用于证实性研究。因此,多重比较各种方法都用一用选P值的做法是不妥的。(26)当例数较少或理论频数较小时,为什么要用校正χ2检验或Fisher精确检验因为χ2检验统计量的抽样分布是矩形分布,χ2分布为连续性分布。利用χ2检验统计量进行列联表差异性检验时是通过用χ2分布作为χ2统计量分布的近似方法进行的。χ2统计量计算结果往往较大,特别是在自由度较小、样本量较少情况下。因此Yetes提出了校正的方法。在实际应用中,当样本含量大于40,理论频数都大于5时,χ2统计量近似性较好,可以不进行校正;但是当存在理论频数小于5时,近似性较差,需进行校正;当例数小于40或存在理论频数小于1时,近似性更差,因此主张改用更合适的Fisher精确检验代替χ2检验。(27)对于多组二分类资料和无序多分类资料,能否通过转化为多个四格表资料分别进行检验?对于多组二分类资料和无序多分类资料,若转化为多个四格表资料分别进行检验,割裂了原来的设计,更重要的是会增加犯Ⅰ类错误的概率。例如对于3X3列联表,检验水准取0.05,若转化为多个四格表资料分别进行检验,应进行9次检验,这样犯Ⅰ类错误的概率将达到1-((1-0.05)9=0.37,远远大于0.05。因此,对于多组二分类资料和无序多分类资料,不能通过转化为多个四格表资料分别进行检验。当多组二分类资料和无序多分类资料检验结果拒绝假设H0时,可以进一步作两两比较,但α水平需要按α/比较次数来校正。(28)对于有序多分类资料,用无序多分类资料方法进行差异性检验会出现什么问题?因为列联表χ2检验的χ2统计量只能处理频数分布的差异性检验,没有处理有序信息的能力,不能利用数据所提供的有序信息进行分析。因此,若使用无序多分类资料分析方法进行有序多分类资料的差异性检验,将会降低统计检验效能。(29) 是否所有资料皆可作相关分析?只要输入数据,电脑就可以进行相关系数的计算,但这不表明任何资料皆可进行相关分析。相关分析要求两变量皆为随机变量,如果X是人为取值,则不宜计算相关系数。计算Pearson相关系数还要求资料为双变量正态分布。同时应注意,资料类型不同,所采用的刻画相关或关联的方法也不同。(30) 程序中自动给出了相关系数值和假设检验结果,为什么还要作散点图呢?的确,有不少研究不作散点图就给出相关系数值和假设检验的结果,但这样做可能会出现两变量间实际没有线性关系而作出线性相关的决定,也可能不容易发现资料有异常值或有分层的情况等。因此,相关分析必须先作散点图,确认有线性关系时才计算相关系数,并对其进行检验。(31) 若两组比较某指标的均数不同,是否可以说明该指标与分组因素相关?要注意“相关”是一个专业用语,有特定的含义。仅均数不同不能认为相关,若各组均数差别有统计学意义,可以认为不同组间总体水平不同。通常所说的“某指标的均数与分组有关”和统计学所说“某指标与分组变量间线性相关”是两个不同的概念。线性相关的结论必须通过相关分析或关联分析才可得到,而分组因素常人为划定,非随机变量,不可作相关分析或关联分析,即便作了计算,也不能得出相关的结论。(32) 经统计检验得出总体相关系数不为0,且P值很小,是否可以认为变量间关系很大?统计检验的P值是指总体相关系数为0时,得到等于或大于目前这个样本相关系数的概率大小。若P值小,说明总体相关系数为0时,不大可能得到目前这个样本相关系数,从而怀疑总体相关系数是否为0。不论P值多么小,结论只能是总体相关系数不为0而已。样本量小时,样本相关系数值很大也可能得出没有统计学意义的结果;反过来,样本量大时,很小的样本相关系数值也可以拒绝零假设。如样本量大于50时,r=0.279就可以得到P<0.05的结果,而样本量为5时,即使r=0.870时仍得到P>0.05的结果。(33) 既然Spearman等级相关对资料性质没有要求,是否所有资料皆可用等级相关?文献确有把Spearman等级相关当成万能相关方法。不管什么样的资料都可用Spearman等级相关方法,但这样做的结果会损失信息,降低功效。因此,应根据资料类型和适用条件选用相关强度指标。当两变量为连续型随机变量时,通常采用积矩相关系数。(34) 计算Spearman等级相关系数时,怎么有人采用公式?实际上,无相同秩次时,此公式与利用秩次采用Pearson相关系数的公式计算时完全等价,但有相同秩次时一般不宜用此公式。此公式为过去计算机不甚普及时推算出的无相同秩次的简便计算公式,有相同秩次时需要校正。(35) 多组比较的RX2表或RXC表和本章的RXC表在设计上有区别吗?多组比较的Rx2表或RXC表,属于完全随机设计资料。多组资料比较的设计是,首先设定组别(如三种国籍人群),各组例数的调整不受其他组别的影响,然后调查各组的频率分布(血型分布)情况,分析各组(三种国籍)的频率分布(血型分布)是否不同。本章的RXC表资料是一次调查的结果,可看作是总体中的一份样本,其样本含量<2500例)是固定的,某属性之一(如国籍中美国人)的例数变动必使该属性其他分类(如国籍中中国人和挪威人等)的例数反向变动,统计时按两种属性(国籍和血型)交叉分类统计频数,得到两种属性是否独立的结果。(36) 如何识别与处理异常点?在实践中,科研工作者鉴别数据中的异常点是进行统计分析前首先要完成的一项工作,否则会导致错误而前功尽弃,得不偿失。有些“统计谎言”正是由于分析者疏忽异常点的存在,夸大或弱化实际效应而造成的,如图10-10,虚线代表受异常点影响而偏离的回归线。异常数据的识别可以通过简单、直观、有效的散点图发现,也可以通过相关统计量(如广义平方距离)获得。通过散点图可直观地反映哪些数据是可能的异常数据。一旦发现可能的异常数据,不宜草率地删除,应该仔细审查这些可能异常数据的获得过程。若是由实验获得的,如有可能应该重新在该点重复作几次实验进行验证。只有当异常数据是由于实验失误、记录错误等人为因素造成的,才考虑删除或以重新测量的正确数据来替代。如果通过仔细审核发现数据的异常值是因数据本身性质造成的,对这样的数据应该引起足够的重视,对它进行另外的研究有可能获得意外的发现。(37)两变量不是线性关系时怎么办?在复杂的生物医学现象中,很多情况是两个变量间的关系呈非线性变化趋势,如血药浓度与时间效应曲线、生长曲线、剂量反应关系等。对于非线性的问题,如果仍一味采用简单的线性回归分析,其直接后果是歪曲实际的变化规律。实际工作中,采用曲线拟合的方法,常用的曲线类型有:1)指数曲线 又称指数生长曲线,双变量资料中,当自变量X增加时,因变量Y随之增加(或减少)得更快,这时可采用指数曲线方程来分析两变量之间的关系。2)多项式曲线 多项式曲线方程为抛物线性,当为一次时则为简单线性模型,模型中加人b2X3、b3X3项,则为二次、三次多项式曲线。多项式适合于标准曲线的绘制。3) Logistic曲线 又称Pearl-Reed曲线,呈拉长的“S“形曲线,多用于发育、动态率、剂量反应关系以及人口等方面的研究,在后面章节中讲到的logistic模型即属于此。4)双曲线与指数曲线相类似,但适用于弯曲程度更大的资料,如肌肉张力、神经生理方面强度一时间数据的分析。SPSS软件可以实现更多的曲线拟合,方便科研工作者应用。实际工作中,应根据散点图尝试拟合多种曲线。如何确定最终的曲线类型,要掌握以下原则:① R2越大,拟合效果越好。但不必过度地追求好的拟合优度,如拟合多项式模型时,虽幂次越高,R2越大,但会给解释上带来麻烦。②要考虑曲线类型是否符合专业解释。③在拟合优度相近的情况下,一般选择容易解释、易于表达的曲线类型。,(38) 两批数据能合并后拟合线性回归方程吗?实际工作中,常有X与Y变量来自于两批数据,不能轻易将两批数据合并后进行回归分析,所分析样本应保证来自一个总体(即保证同质)。如果两批数据来自两个不同的子群,可能得出不符合实际的结论。如图10-11所示,实点与虚点分别代表两批数据,图10-11a中实际不存在的回归关系,合并后被误认为有回归关系;图10-11b有可能存在回归关系,合并后会被误为无回归关系。在此,两个子群成为影响回归关系的混淆因素。电脑实验(实验10-4)中对盲目合并数据误导专业结论的情形进行了数据模拟分析。对这类数据需要进行分组分析或在多重线性回归分析中引入交互项的办法来分析处理,分析方法参见第11章。(39)如果反应变量是有序的或分类的变量,应该怎么办?多重线性回归分析要求在固定自变量的情况下,反应变量Y是服从正态分布的连续型随机变量(也就是残差服从正态分布),如血压值、身高、体重等。但是,在医学研究中,一些反应变量往往是分类变量。例如,心功能的分级就是一个有序分类变量,虽然各级之间有程度上的差别,但是1级(体力活动不受限制)和2级(体力活动轻度受限)之间的差别并不等同于3级(体力活动明显受限)和4级(不能从事任何体力活动,休息时亦有症状)之间的差别。也即这里的数字1,2,3,4仅仅代表不同的等级,并不代表实际的数量大小。另外,无序的分类变量在医学研究中也很常见,例如治疗的结局分为治愈和死亡。当反应变量是有序或无序的分类变量时,不能采用多重线性回归对资料进行多因素分析,可以考虑采用logistic回归等其他多因素分析方法。(40)自变量存在缺失数据时怎么办?进行多因素分析时,如何处理缺失数据是一个常见的问题。所谓缺失数据,常指观察对象在某些变量上的数值缺失,例如缺少年龄、性别或者血压值等方面的信息。缺失的原因可能是偶然的、随机的,如调查时由于疏忽漏填了;也有可能是系统性的,如由于疾病恶化而没有提供信息。对于有缺失数据的观察对象,不能简单地删除。人们针对缺失数据常见的处理方法是:1)尽量了解缺失的原因,尽量弥补缺失的数据。2)对每个自变量考察缺失数据的多少。3)如果有一两个自变量的缺失数据较多,考虑删除该自变量。无论自变量在专业上意义如何重大,如果存在大量的缺失数据,则结果极可能存在偏倚。4)如果极少的观测有缺失数据,可以在分析前删除这些观测。5)如果大量观测有缺失数据,应该分析有缺失数据的观测和没有缺失数据的观测之间的差别,也即考察缺失的原因是随机的还是非随机的。如果有缺失数据的观测组成的样本的基本情况与没有缺失数据的观测组成的样本的基本情况无差别,则称数据的缺失是随机的,反之,为非随机缺失。如果数据的缺失是随机的,可以采用完全数据的均数填补缺失数据。如果数据的缺失是非随机的,应分别分析有缺失数据的观测组成的样本和没有缺失数据的观测组成的样本资料,且下结论需慎重,以防止偏倚。(41) 自变量筛选是必须要做的吗?前面介绍了多重线性回归分析中自变量筛选的统计学标准和筛选策略,那么在实际应用中自变量的筛选是必须要做的吗?有时并不是必须要做的,有时又是必须要做的。是否进行变量的筛选取决于专业的理论、经验以及资料的实际情况。最后得到的模型不仅要符合统计学的要求,更重要的是从专业上得到合理的解释。(42)如何判断是否存在多重共线性一种简单的方法是计算所有自变量的相关系数矩阵。如果两个自变量之间的相关系数超过0.9,则会带来共线性的问题;如果相关系数在0.8以下,一般不大会出现问题。另外,统计学家还提出了两个帮助判断是否存在多重共线性问题的统计量,它们分别是方差膨胀因子(variance inflation factor, VIF)和容忍度(tolerance)。下面简单介绍VIF的原理和计算方法。假定有p个自变量,依次把每一个自变量当作反应变量与余下的p-1个自变量进行多重线性回归分析。表示当第j个自变量被当作反应变量时多重线性回归方程的确定系数,j=1,2,…,p。针对每个多重线性回归方程,VIF定义为:如果第j个自变量与余下的p-1个自变量相关密切,则接近于1,VIFj会较大。研究结果提示,当VIF>4时,可能存在共线性问题;如果VIF>10,则共线性问题严重。容忍度是VIF的倒数,因此如果容忍度小于0.25,则可能存在共线性问题,如果容忍度小于0.10,则提示共线性问题严重。(43)如果实验条件满足配对设计要求,研究者却采用了成组设计,这将意味着什么?如果实验条件不满足配对设计要求,研究者却一定要套用配对设计,又将意味着什么?如果实验条件满足配对设计要求,即能够找到对观测结果有影响的重要非实验因素,而且受试对象可以按此非实验因素进行配对,此时研究者却采用了成组设计,这将意味着人为增大了实验误差,易导致假阴性结果的出现;如果实验条件不满足配对设计要求,即无法找到对观测结果有影响的重要非实验因素,此时研究者却一定要套用配对设计,实际上各对受试对象除处理因素取不同水平外,在其他方面相差悬殊,若按配对设计方法处理实验数据,将意味着人为降低了实验误差,易导致假阳性结果的出现。(44)单因素设计简便易行,可以通过随机化方法平衡其他因素对单因素各水平组中观测结果的影响,是否可以不考虑任何多因素实验设计方法?在进行实验设计时,通常涉及两类因素。其一,研究者关心的实验因素;其二,研究者不关心但客观上会影响观测结果取值的因素,比如区组因素。当某实验仅涉及多个实验因素,且实验因素的数目大于等于2时,若在实验设计时将其他实验因素控制在各自特定的水平上,每批实验只允许一个实验因素取不同水平,即采用单因素设计取代多因素设计的作法是不够妥当的。若希望通过实验研究,弄清多个实验因素之间的相互关系,通常情况下以选用析因设计为宜。(45)在实验设计中,对照组的设立十分重要,一般来说,应设立几个对照组合适?在实验设计中,应设立几个对照组不便一概而论,主要取决于实验研究的目的和涉及的实验因素的个数。①如果是标准的单因素多水平设计,通常只需要设立一个对照组即可。例如,希望考察某药物取小、中、大三个剂量所产生的疗效之间的差别是否具有统计学意义,当对此药物的疗效一概不知时,需要设立一个空白对照组,即采用单因素4水平设计;当已知该药开始起效的最低剂量时,可以不设立空白对照组,该药物的小、中、大三个剂量组互为对照,即采用单因素3水平设计即可。②在某些实际问题中,有人常设立多个对照组,如正常(或空白)对照组、模型对照组、阳性药对照组,其他是研究者所研究的新药取几个不同剂量的实验组。③如果是标准的多因素实验设计,所有组都有其特定含义,往往是同一个实验因素各水平组之间相互对照,如多因素析因设计。(46) 在实验设计中,如何根据情况选用合适的实验设计类型?这是一个比较复杂的问题,只能概括地讲一下选用的基本原则。如果在实验中研究者关心的实验因素只有一个,来自受试对象的各种重要的非实验因素的影响可以通过完全随机化方法使之在实验因素各水平组之间达到均衡一致,则可以选用单因素k水平设计((k=2时为成组设计,k=3时为单因素多水平设计);如果在实验中研究者关心的实验因素只有一个,但来自受试对象的各种重要的非实验因素的影响无法通过完全随机化方法使之在实验因素各水平组之间达到均衡一致,则应考虑选用随机区组设计或交叉设计;如果在实验中研究者关心的实验因素的个数大于等于2,来自受试对象的各种重要的非实验因素的影响可以通过完全随机化方法使之在实验因素各水平组合之间达到均衡一致,则可以选用析因设计。析因设计需要的实验次数较多,如果实验经费、时间和人力等都很难达到要求,可考虑选用其他多因素实验的设计方法,请参阅实验设计专著。(47) 在进行新药临床试验时。无论从形式还是从内容上,都严格按我国《新药注册管理办法》中明文规定的要求去做,是否是最正确的?由于相当多的研究者对Ⅱ、Ⅱ期临床试验的本质理解不够深入,又由于国家审评部门对新药临床研究的要求过于简单和格式化,导致绝大部分临床试验都照搬《新药注册管理办法》的基本要求,试验方法和类型千篇一律,无法妥善处置可能遇到的特殊问题。应该采取实事求是的态度,在原则问题上严格按国家有关规定办理,而对于各种情况下遇到的具体细节问题,应从多种处置方案中选择最优者。(48) 在进行新药临床试验时,可否直接按我国《新药注册管理办法》中明文规定的样本含量的最低要求来确定样本含量?多数临床试验没有进行样本含量估算,而仅仅按照《新药注册管理办法》对病例数的最低要求来做,致使一部分研究不能得到有说服力的结论。应根据预试验或借鉴他人经验信息,获得有关本试验研究所需要的基本信息,选用合适的估计样本含量的公式或专业软件估计出样本含量N。当估计出的N大于《新药注册管理办法》对病例数的最低要求时,就以N为样本含量;反之,应按《新药注册管理办法》对病例数的最低要求确定样本含量。(49) 在进行新药临床试验时,如何正确选择评价指标?评价指标的选择是临床试验的核心问题,应当在清晰确定临床试验目的的基础上,根据临床医学专业知识,选择最恰当的评价指标。应当充分重视终点指标和实验室替代指标,慎重使用综合指标和难以定量的指标(主观性指标),切忌试验目的不明确,以多指标为主要评价指标的大撒网式研究。(50)在进行与中药有关的新药临床试验时,应着重考虑的问题是什么?中药作为中国创新药品的重要源泉,其临床试验在评价指标选择和评价方法上存在很多争议,致使中药临床试验结论很难与西医或国外进行沟通。因此,应着重考虑的问题是评价指标的选择和评价方法的确定,即评价对象和评价工具保持一致,才有可能相互比较、沟通和理解。(51)在进行新药临床试验时,数据管理至关重要,应在哪些方面把好质量关?目前在中国的临床试验中,数据管理的三个要点(准确、及时和安全)难以高品质地实现。在这方面,应进一步提高认识,建立健全操作规程,严格按操作规程进行质量监督和检查。(52)临床试验质量控制非常重要,它包括哪些方面呢?通常,临床试验质量控制包括检查、稽查、视察、研究者控制、数据管理和统计分析控制,在这些方面,我国的临床试验质量控制水平尚没有达到国际要求,存在着试验数据有可能失真的隐患。(53) 在调查研究中,如何控制和保证调查质量?在调查研究中,主要从以下几个方面进行质量控制,以保证调查结果的可靠性:1)现场调查工作阶段的质量控制。2)资料整理、表达与统计分析阶段的质量控制。3)偏倚的控制。(54)在调查敏感性问题时,如何能获得比较真实的答案?在调查研究中,有时需要了解一些隐私问题(包括心理、行为、与“性”有关的问题等)。当询问此类问题时,调查对象往往不愿意回答或给出的答案是不真实的,这类问题统称为敏感性问题。在调查敏感性问题时,要想获得比较真实的答案,需要打消调查对象的思想顾虑。首先,调查表或问卷上应当是无记名的;最好调查者不在现场,在一个未安装监视器的大厅内(室内外无其他人),调查对象将填好后的调查表投人加锁的投票箱内;更让调查对象放心的方法是他们回答的是敏感问题还是非敏感问题,调查者一概不知,更不用说他们对敏感问题作出的是肯定还是否定的回答了,实现后者的调查技术需要较深的概率论知识。(55) 希望说明一种新药物或新疗法是否优于常规药物或疗法,请问:我应当采用多大的样本?这是相当多的研究者在进行科研工作之前经常提出的问题,但又是无法回答的问题。因为估计样本含量需要很多信息,第一,要知道所作的研究属于何种研究类型,实验设计、临床试验设计和调查设计所用的样本含量计算公式是不完全相同的;第二,即使是实验设计,还涉及拟解决问题的复杂程度;第三,需要给定与拟解决问题对应的一些基本信息。凭空估算样本含量是没有科学依据的,因而也是无意义的。(56) 样本较小时结论不可信,是否样本特别大时结论就一定可信?不一定!要看拟解决的问题的复杂程度和对重要非实验因素的控制质量。若实验研究涉及多因素多水平设计问题,即使总样本含量特别大,但分到每个小组中去的受试对象的个数却很小时,其结论仍是不可信的;若实验研究涉及单因素多水平设计问题,但由于许多重要的非实验因素对实验因素各水平组的影响很不均衡,即使各组样本含量均较大,其结论也是值得怀疑的,甚至是错误的。(57)是否有办法使一项科研工作的结论同时犯假阳性错误和假阴性错误的概率都很小?比较好的办法是: 提高统计研究设计的质量和研究过程的质量控制水平,同时,使各小组具有足够的样本含量,组间具有很好的均衡性。(58) 我不想论证两种药物疗效之间的差别,而是想说明两种药物效果差不多,从而一种较便宜的药物便可以取代另一种较昂贵的药物,这时,样本量该怎么考虑?此时,研究的目的叫作“等效性检验”,应根据此类检验对应的样本含量估计公式进行估计,请参阅有关专著。(59) 对于一个随机区组设计资料,我们既用单因素方差分析,也用两因素方差分析,发现假设检验的结论一致,难道用单因素方差分析不可以吗?并且计算简单。不可以。对于随机区组设计资料,尽管用两种方法分析的检验结论可能多数情况一致,但两因素方差分析可从总变异中分解出处理因素和区组因素导致的变异,单因素方差分析只从总变异中分解出一个因素所致的变异,因此与单因素方差分析的组内变异相比,两因素方差分析的误差变异减少了其他因素对随机误差的影响,更接近真正的“随机误差”,因此据此计算F统计量并推断更准确合理;另外,单因素方差分析检验效能较低。(60) 当经方差分析认为析因设计资料中某因素的主效应有统计学意义,而交互效应无统计学意义时,欲知哪个水平最好,应如何分析?如何选择最佳的实验组合?当该因素水平数超过2时,可以对该因素不同水平间的主效应作多重比较,比较的方法可参见《医学统计学》(余松林主编,人民卫生出版社,2002)第110页。选择最优实验组合时,当因素间交互效应差异无统计学意义,而各因素均有统计学意义时,则各因素最佳实验水平的组合即为最优实验组合;如果某因素无统计学意义,则从中选择经济、简便、无(低)痛苦、无(低)不良反应的实验水平。(61 )析因设计资料经方差分析后某两因素的交互效应有统计学意义,如何选择实验条件?可通过对各种实验组合的多重比较选择实验条件,比较的方法可参见《医学统计学))(余松林主编,人民卫生出版社,2002)第110页。当两种组合间比较差异有统计学意义时,选择实验效果更佳的实验条件;若差异无统计学意义,则选择经济、简便、无(低)痛苦、无(低)不良反应的实验组合。(62) 交互效应与交互作用有何不同?如何判断实验因素间有无医学上常说的拮抗作用和协同作用?交互效应是指在方差分析中描述交互作用项的参数,对于多因素的实验性研究中,研究因素的各个水平是有序的,代表了每种干预的强度,如果两个因素主效应均大于0,则其交互效应>0,说明两种干预的叠加效应大于两种单独干预的效应之和,故称为协同作用;反之,如果两个因素主效应均大于0,而其交互效应<0,说明两种干预的叠加效应小于两种单独干预的效应之和,故称为拮抗作用。(63)在重复测量设计的方差分析中,处理效应是什么?在同样的其他条件下,不同处理所对应的观察变量的总体均数差异,在例17-1中的处理效应是试验药与对照药治疗慢性乙型肝炎的ALT总体均数差异。(64)在重复测量设计的方差分析中,时间效应是什么?时间效应是指在同样的处理和其他条件下,观察变量的总体均数随着时间变化所对应的差异。在例17-1中的在同为试验药或对照药治疗慢性乙型肝炎的情况下,ALT总体均数随着时间变化所对应的差异。(65)在重复测量设计的方差分析中,处理效应与时间效应的交互作用是什么?如果不同处理所对应的总体均数之间的差异随着观察时间变化而变化,则称为处理效应与时间效应有交互作用;反之,如果随着观察时间的变化,不同处理所对应的总体均数之间的差异是个常数(即不随观察时间变化而变化),则称处理效应与时间效应无交互作用。在例17-1中,统计推断的结论为:两组所对应的ALT总体均数之差不随观察时间变化而变化,故该例的处理效应与时间效应无交互作用。(66)在重复测量设计的方差分析中,能否用治疗前后观察值的改变量作为评价指标?用治疗后观察值作为评价指标是描述受试者在治疗后的症状水平。治疗前后的观察值改变量作为评价指标是描述治疗后症状改变的程度。在许多情况下,两者均可以作为评价指标,并且治疗前后的改变量往往有时更能体现药物疗效功能,但当治疗后的受试者处于治愈或恢复到正常状况时,用治疗前后的观察值改变量作为评价指标就存在一些问题了。例如:评价感冒药的疗效,观察指标为感冒的各种症状总分,当感冒治愈时,各种症状总分为0,这时治疗前后的观察值改变量一治疗前的各种症状总分一0分=治疗前的各种症状总分,因此,治疗前后的观察值改变量作为评价指标就成为治疗前的症状总分评价,这时治疗前后的症状总分改变量不能反映疗效的问题了。在例17-1中,几乎所有的受试者在第36周的ALT测量值都属于正常范围,因此ALT观察值在正常范围内的波动属于个体变异,与药物的疗效关系不太大。因此,用治疗前后的ALT改变量作为评价指标就不能较好地反映临床治疗效果,如果两组的治疗前的观察值平均水平是无统计学意义的,则用各个时点的ALT观察值反映药物治疗能使受试者的ALT达到何种水平和范围就有较好的临床意义。(67)连续型定量变量如何引入回归模型?连续型定量变量若直接以定量变量形式引入方程,对于定量变量与logit π呈线性的情况下,可以减少信息损失,减少方程增设哑变量个数,增大检验效能,但当该变量与logit π没有近似线性关系时,反而导致参数估计误差加大,甚至结果无法解释。所以,对于这种情况,一般采用离散化的方法,以哑变量形式引入模型。离散化类别的个数一方面要依据专业知识,另一方面要根据样本量及拟纳入方程分析的自变量个数确定。(68) 如何建立好的回归模型?研究者通过统计软件,采用逐步前进法或后退法,逐个入选或剔除自变量,建立logistic回归模型。这种作法从统计学意义上无可厚非,但是统计回归模型的生命力在于解决实际问题,回归模型必须要“工作”。从应用角度看,完全依赖统计软件筛选自变量,建立回归模型的作法有片面性。要将专业经验与统计学原理、方法相结合,认真筛选进人方程的自变量,以建立好的统计回归模型。当采用统计学与专业知识结合的方法,筛选进人方程的自变量还不满意时,可以考虑对常用logistic回归方程进行必要的修改,如方程中增加变量的二次项或相关自变量的交互项等,使拟合方程更加符合客观实际。(69) 如何计算有交互效应时的优势比?以只有两个自变量的logistic方程为例。没有交互效应的模型(即主效应模型)为logit π=β0+β1X1+β2X2。如果考虑X1, ,X2。间存在一阶交互效应,模型表达式为logit π=β0+β1X1+β2X2+β3X1X2,当因素X1增加一个单位,即=X1+1,其他条件不变时的优势比为。一般要讨论不同的X2取值,检验β1+β3X2=0的问题。如X2= 0,则OR1=exp(β1),检验H0: β1=0;如X2 =1,则OR1=exp(β1+β3),检验H0: β1+β3=0。因此,有交互效应时X1的优势比不是一个常数,它还取决于另一因素的状况(自变量X2取值)。
 活菩萨
活菩萨医学研究资料收集与整理的基本要求
一般来说,在研究实施后,就要围绕研究主题着手收集并积累相关材料,然后根据相关的统计学方法进行整理,以便后续的分析研究。对于医学研究论文而言,材料收集与整理是撰写高质量论文的重要条件,但论文材料来源于科学的课题设计和恰当的实验方法,所以研究的科学性、创新性、合理性才是完成高质量论文的基础。医刊汇编译指出,医学研究资料收集与整理的基本要求有:真实、系统、完整、典型、新颖,同时要符合 伦理学的要求。1.材料的真实是对论文资料最基本的要求,只有从真实的资料中才能发现其蕴含的内在规律,若是从不真实的材料或随意编造的数据中总结规律,得出的结论必然是错误的,这种错误不仅无助于临床决策,还有可能导致临床决策失误,进而威胁患者生命安全。因而要尊重事实,从真实的资料着手科学研究。2.医学研究的对象通常是复杂并相互联系的,这就要求反映研究对象的资料有系统性和完整性,才能从整体上揭示事物的本质和规律,才能对研究对象有较深刻的认识。系统和完整不仅指研究样本的数量要达到统计学要求,而且每个样本的信息也必须全面,不能遗漏项目,否则可能使统计结果出现偏差,导致错误结论。3.材料必须符合论文主题的要求并具有较强的代表性和说服力,所以选用的材料要有典型性,要善于从众多繁杂的材料中选取具有代表性的材料。4.创新性是研究者创造性劳动的体现,所以在收集材料时要特别注意对新发现、新思路的及时记录;并要广泛收集文献材料,从中选取能反映新进展、新成果的新材料,将这些具有新颖性的材料纳入论文之中。5.医学研究的目的在于促进人类对疾病的认识水平,进而提高诊疗水平,改善人类生存状态。医学科研的目的是为了维护和增进人类健康和造福于人类,因而医学科研不同于其他学科科研活动的关键在于,它总是直接或间接地为人的生命和缝康利益服务,所以不管医学科研工作者是否意识到,整个医学科研活动都会始终在人类道德天平上,接受道德检验。因此科学研究应注重研究对象的利益、符合伦理,在进行人体或动物的生物医学研究时,要经过相关医学伦理委员会的审查,以维护研究活动参与者的尊严、权利和安全。在收集资料时应向研究对象说明来意,征得同意后才能开始收集资料;当研究涉及个人隐私时,更要尊重研究对象的要求。
 飞行猫
飞行猫数据分析:浅谈统计学在生活中的应用,看完长见识了!
浅谈统计学在生活中的应用统计学并不是一门独立存在的学科,它是以数学知识和数理统计作为基础,将数理统计方法和其他学科专业知识交叉融合形成的具有极强推断性的一种分析方法。现阶段,随着科学技术的快速发展,为了加强对自然社会各个领域现象的判断和整理能力,将统计学应用在生活各个方面已经成为现阶段的数理统计的一种便捷方法。 一、统计学的概念 统计学指的是调研人员通过一些列的手段对整理出来的数据信息进行整理分析,从而推断出调研对象本质,甚至可以对未来的类似事情进行预判的一门综合性学科。在进行统计学整体分析的过程中需要用到大量的数学知识以及其他相关学科的专业知识,统计学由于其自身独特的性质,在社会科学和自然科学的各个领域几乎都可以使用。 二、统计学在生活中的应用分析 (一)统计学在经济学中的重要应用 运用统计学对生活中的数据信息进行整理分析,首先要学习统计学的基础知识以及数据统计个分析等学科,这些基础知识和方法都是在开展统计学应用活动之前调研人员所必须掌握的。统计学课程的学习作为经济学学科当中的重要分支,在经济学课程中经常被应用,例如,经济学的计量统计就需要根据统计学在金融里面的重要意义和地位作为基础,将金融知识和统计学知识相结合,将金融计量和时间的序列进行结合,对收集到的金融数据进行整理分析,最后得出金融计量和时间序列的一定关系。 统计学在金融经济学中有着十分重要的工具性作用,主要包括两个方面,分别是:在思想上而言,统计学是对数据统计分析结果进行研究,最后得出研究对象的判断结果,为了保证研究结果的准确可靠性,统计学在进行数据整理分析过程中必须是带着严谨的科学态度,这种严谨的科学态度对于经济学的相关理论分析具有十分重要的指导地位,这是由于研究人员在对金融量进行数学分析的过程中,为了保证金融数学分析结果的准确可靠性就必须保证金融量数据收集分析等预处理过程是科学合理的;其本收集整理次,统计学是经济学进行科学试验研究最优化的选择,经济试验研究活动的多样性以及研究对象之间错综复杂的关系导致经济学的试验研究活动受到诸多限制,运用统计学进行经济学试验研究活动,使得经济学实验研究的对象变得简洁明了,降低试验研究的成本支出。从统计学在经济学中的应用我们可以看出,经济学当中的统计学应用主要是运用了统计学当中经济必然性的思想,使得经济学当中的统计结论不具备复杂的思想成本。 (二)统计学在医学中的重要应用 统计学在医学中应用的主要原因就是生物医学中存在的不确定性和变异性。生物医学主要的研究目标就是与人体健康相关的不确定因素,也就是通常所说的医学变异现象,变异现象在生物体当中是普遍存在的,例如,对于外在条件基本相同的两个病人,在相同的条件下进行治疗时,却有可能出现有的病人被治愈,有的病人治疗效果不明显,甚至还会出现死亡的现象。造成这些外在条件相同的生命体却出现不同程度治愈的主要原因就是生物医学中存在的不确定性或者是人体中存在的错综复杂的随机因素,客观差异存在的原因是因为某种偶然性的潜在的揭露必然性的发现。 在医学临床统计中发现,对于同一种病因的客观性规律进行调查,对于健康人的共同作用的交织与疗效的考查的病人很少。在医学当中运用统计学最主要的就是通过观察不同疗效病人的医疗诊断效果,将实际的医学诊断治疗效果与医学理论和假设进行验证,运用概率论以及数学方法对对比结果进行分析、判断,运用电子计算机等相关软件设备对研究对象的指标进行记录,并绘制相应的图表等,通过综合运用多种数理统计方法,得出与研究对象相关的研究结果。将统计学应用到医学当中,可以促进统计方法和多变量分析法在医学试验研究中的应用,对未知病因所造成的医疗诊断事故进行分析,可以促进医疗诊治手段的不断创新發展。 (三)统计学在体育比赛中竞技指标的应用。 统计学在体育比赛中的应用主要是用统计的职业联赛的数字反应比赛队伍能否成为世界顶级,这是因为在体育比赛中应用统计学可以对比赛中的胜率进行分析,主要是将每个队员在每个赛季比赛的分数和常规赛场上的分数进行统计,通过一系列的数学计算分析,制定出每个队员得分平均值和标准差之间的正态分布图,通过正态分布图的稳定性来判断队员的技术稳定性。以众所周的NBA篮球比赛为例,NBA比赛中由于明星球员众多,在运用统计学进行数据整体分析时,需要依据本质上的规律进行数据统计,而不是随意的选择数据进行统计,例如在进行篮球比赛发球这一项双方队员的进攻和防守的概率时,在进行指标选择时就涉及到随机事件的发生概率,因此,可以运用统计学统计球员在每一场比赛上的均得分,通过这些数据指标的正态分布图来确定球员的技术稳定性。 三、结束语 在日常生活中应用统计学对数据进行管理分析,可以极大提高生产生活中对研究对象的管理效率,使得研究对象变得明确,降低管理成本。在实际的生产生活中应用统计学时,调研人员需要通过多次的试验和随机概率对比来确定事件发生的概率,通过定量定性的数理统计分析工作,充分发挥统计学对生产生活的促进作用。
 法琳
法琳南科大新成立的生物医学统计中心将给深圳带来什么?
南都讯 记者朱倩10月23日下午,南方科技大学生物医学统计中心揭牌。生物医学统计中心旨在建成具有国内一流水平和国际影响力,集基础研究,多学科交叉融合,咨询,专业人才培养以及产业转化为一体的综合科研基地。南科大代理副校长方复全致辞中表示,深圳在生物医学领域已基本形成较为完善的生物医药产业链和空间链,但对专业人才的需求仍十分迫切。依托粤澳港大湾区的地缘条件以及南科大的学科和人才优势,相信生物医学统计中心的成立能整合相关领域方面人才,创建具有国际水平的综合科研基地,实现学界与业界的跨界合作共赢。揭牌仪式上,史建清获任命南科大生物医学统计中心主任。南科大副校长方复全院士、理学院院长杨学明院士分别致辞,对中心成立表示祝贺。揭牌。跨学科开展研究已针对帕金森综合征可穿戴带设备举行数据收集与建模据了解,该生物医学统计中心作为南科大理学院下设的一个高层次高水平的科研机构,将集中在复杂性数据分析(包含精准医疗和公众健康研究)、适应性临床试验和数据分析、统计组学数据分析(包含生物学、高效计算技术)等方向的研究,并与南方科技大学医学院、生物系、化学系、深圳应用数学中心,南方科大医院,深圳市儿童医院等科研机构和院系建立紧密联系,联合开展生物医学领域的研究,创建一流的数据分析实验室。在产业应用方面,中心将面向生物医药相关企业提供生物统计学相关的咨询服务,为企业和大学创造价值。据悉,该中心已与南科大医院神经内科合作,聚焦帕金森综合征可穿戴带设备的数据收集与建模,为患者提供早期诊断和临床监测等服务,并进行生物信息学与健康数据融合和药物开发的研究。方复全线上致辞。杨学明史建清将利用深圳各项优势建成一流的研究基地此外,南科大理学院院长杨学明在致辞中表示,生物医学统计中心作为一个高层次平台,可以充分利用南科大和深圳市的各项科技及人才优势,能够最大程度地调动资源,推动交叉学科理论研究开展、产出高水平科研成果、培养具有多学科背景的复合型人才、建成一流的生物医学统计研究基地,为生物和医疗技术提供发展及解决方案。生物医学统计中心教授史建清在发言中表示,中心将依托于学校的优质资源与人才优势,促进统计系与南科大医学院、生物工程系、深圳应用数学中心,正在建设中的公共卫生与应急管理学院等院系机构建立紧密联系,发展创新理论和技术,探索对生命健康数据的分析和解释;重视交叉学科建设,攻克生命科学中的实际问题;推动复杂数据和大数据的创新研究,探索根本,创造价值。本次揭牌仪式邀请到中心顾问委员会的英国纽卡斯尔大学Robin Henderson和美国耶鲁大学Hongyu Zhao两位国际顶级教授做大会专题报告,线上分享了生物医学统计相关领域最新的研究思想和成果。【来源:南方都市报】声明:转载此文是出于传递更多信息之目的。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 邮箱地址:newmedia@xxcb.cn
 是无内也
是无内也利用生物和统计协变量提高数据分析统计效率
原文以 Leveraging biological and statistical covariates improves the detection power in epigenome-wide association testing 为标题发布在 Genome Biology 期刊上海交通大学医学院附属瑞金医院黄金艳研究员与梅奥医学中心陈军研究员合作,使用模拟和真实的表观基因组关联分析数据集,使用数据集对应的协变量,评估了五种FDR控制方法的性能。该研究开发了一个综合测试来评估协变量的有效性,分析发现统计协变量通常比生物变量能更好的控制假阳性率,并于近日发表在开放获取期刊Genome Biology 上。高通量技术产生海量数据,大大推进了疾病研究的进展,但如何控制对应的生物数据统计检验的假阳性率,提高统计效能一直没有得到很好的解决。比如在表观基因组关联分析(Epigenome-wide association study,EWAS)研究中,需要在表观基因组层面比较不同表型之间的差异,研究通过检测整个基因组成千上万特异DNA核苷酸上甲基的分布情况,鉴别出和表型相关的表观变化。该计算过程中,就涉及成千上万次统计假设检验。假阳性率(False Discovery Rate,FDR)控制广泛应用于校正EWAS假设检验的P值。然而,传统的FDR控制方法,由于其产生时并非针对生物医学大数据的分析,不使用辅助协变量,很有可能不够充分有效地挖掘其中的价值。上海交通大学医学院附属瑞金医院黄金艳研究员与梅奥医学中心陈军研究员合作,使用模拟和真实的EWAS数据集,使用数据集对应的协变量,评估了五种FDR控制方法的性能,这五种方法分别为:Adaptive p value thresholding (AdaPT), Boca and Leek’s FDR regression (BL), covariate adaptive multiple testing (CAMT), FDR regression (FDRreg)和Independent Hypothesis Weighting (IHW)。研究中,开发了一个综合测试来评估协变量的有效性,分析发现统计协变量通常比生物变量能更好的控制假阳性率。甲基化平均值和方差对应的协变量,几乎在各个数据集的分析中,都能取得好的效果。而生物协变量只在某些特定的数据集能有好的作用。研究证明了独立假设加权(Independent Hypothesis Weighting,IHW)和协变量自适应多重测试(Covariate Adaptive Multiple Testing,CAMT)方法总体上更强大,特别是对于稀疏信号,与实际数据集相比,可以将检测能力提高25%和68%。在更大的模拟和实际数据集中,该结论得到进一步的证实。Genome Biologydoi:10.1186/s13059-020-02001-7
 电车狂
电车狂医药生物行业深度研究报告(88页)
(获取报告请百度搜索“未来智库”,登录下载。)展望 2020 年,我们看好医药行业的结构性投资机会 2.0 版。看好创新药、CXO、仿制药产业链上游、疫苗、医疗器械、医疗信息化、连锁医疗及药房等赛道。明年发生变化的是投资可能 向纵深发展,我们建议坚定持有核心资产,同时积极关注具备性 价比优势的细分龙头。新的人口结构下,未满足的临床需求仍然是最核心的投资逻辑未来的 20 年,中国的老龄化将更严重,未满足的临床需求仍然是最核心的投资逻辑。①新的“老年人”将更 多:1963 年至 1973 年的出生高峰期人口全部进入老年阶段,简单计算目前 40 岁至 59 岁人群将逐步进入老年 阶段,这部分人群目前占比达到 30.82%,远高于目前 60 岁以上人群年龄比例(17.87%); ②新的出生人口将更 少:从目前人口结构看,目前 20 岁至 39 岁女性占总人口的 14.32%,而 0 岁至 20 岁女性占总人口的 10.11%, 未来 20 年主要生育女性将减少,在假设生育意愿与生育率保持不变的情况下,新的出生人口仍将更少。根据我 们估算,2028 年 60 岁以上老年人占中国总人口比例可能达到 25%。人类对健康的追求不断提升,亦推动行业 创新步伐,其中未满足的临床需求永远是医药行业最核心的投资逻辑。人口结构变化:新生人口或持续下降,老龄化趋势明显根据 2018 年的死亡率计算逐年死亡人数,由于缺少分年龄段的死亡率数据,我们假设死亡均发生在 60 岁 以上老年人群中。根据预测的新生人口数量以及死亡情况,至 2028 年,60 岁以上老年人占比达到 25%。出生人口减少与健康状态改善,中国人口结构发生巨大变化。过去 15 年中,中国的人口年龄分布发生的巨 大的变化;2003 年,60 岁以上人口占全国总人数的 12.31%;2018 年,60 岁以上老人占比达到 17.87%。一方面 出生人口减少;另一方面,整体健康状态不断改善,中国人的预期寿命在 2000 年为 71.40 岁,至 2017 年已经 达到 76.47 岁。未来的 20 年,中国的老龄化将更严重。退休与住院为医保支出核心方向,老龄化趋势下统筹基金承压。以 2018 年全国职工医保参保人员医疗费用 支出情况为例,退休人群医疗费用较多,使用医保基金也相对较多,人口老龄化进一步加重的情况下,医保基 金所承受压力加大;另外,从门诊/住院的角度看,住院支出占总支出的 62%,如何管控住院费用也是医保关心的核心问题。未满足的临床需求仍然是最核心的投资逻辑人类对健康的追求不断提升,亦推动行业创新步伐,其中未满足的临床需求永远是医药行业最核心的投资 逻辑。产业政策:顶层制度设计明确,对行业投资有重要指导意义医改顶层制度设计基本明确,对行业投资有重要指导意义。11 月 29 日,国务院深化医改小组发布《关于 以药品集中采购和使用为突破口 进一步深化医药卫生体制改革的若干政策措施》,主要从药品、医疗、医保改 革和行业监管四个方面提出了 15 项改革举措。文件要求深化医疗、医保、医药“三医”联动改革,再次明确了“腾 空间、调结构、保衔接”的改革路径,鼓励探索药品/高值耗材集中采购,医疗服务价格动态调整,以按病种付 费为主的多元复合式医保支付方式改革等改革措施,医改顶层制度设计基本明确,对行业投资有重要指导意义。药品集采:国家层面规则预期明确,主要不确定因素在于地方规则国家层面规则不断优化,未来集采将常态化,预期较为明确。三轮带量采购规则不断改进:从最低价中标 到淘汰赛,政策漏洞被不断修补;带量采购模式基本固化,预计未来将常态化,同时采购周期有可能缩短,比 如季度、半年进行集采招标,整体采购频率取决于 CDE 过评企业数量。另外,国家药监局在 9 月底发布《注射 剂一致性评价技术要求(征求意见稿)》,等待正式文件发出,注射剂一致性评价即将启动,后续也会逐步纳入 集采范围。明年主要不确定因素在于地方招采规则。目前政策鼓励地方进行集采创新,构建全国药品公共采购市场和 多方联动的采购格局,未纳入国家采购范围的药品,依托省级采购平台开展集中采购。11 月-12 月已有湖南、 河北、河南濮阳、湖北武汉等地陆续开展地方集采。从治疗领域看,目前涉及抗生素、降压药、降糖药、PPI 等常用药领域;从剂型来看不仅有口服常释剂型, 也拓展至注射剂;另外,目前地方集采的边界也延伸至非一致性评价产品;同时,还有部分地区对自费药品开 展集采,如河南濮阳,根据全市公立医疗机构上年度药品使用情况,遴选出采购金额高、数量大的 200 个品种 以及基础输液类药品进行集采。在地方集采过程中,药品也有较大幅度的降价,以河北为例,13 个拟中标药品 在最高限价的基础上降价 0.3%-80.4%,平均降价 44.5%。在地方集采的示范效应下,各地集采进展很可能会不断突破之前市场预期,对企业的考验也在不断加大。积极创新转型是企业发展的重要方向。医疗:提高医疗服务价格,体现技术劳务价值三医联动,医疗是关键的一环。由于医疗的复杂性和医患知识差异,医生在很大程度上是患者决策的代理 人,完善医院运行机制和薪酬制度可以使医院、医生全心全意为患者的利益提供治疗。医改小组支持各地在开 展药品耗材集中采购、取消医用耗材加成的同时,及时相应调整医疗服务价格,支持公立医院运行机制和薪酬 制度改革;落实“两个允许”要求,增加医院可支配收入。医疗服务价格管理逐步放松,目前积极理顺医疗服务比价关系。我国公立医院医疗服务一直都是由政府定 价或政府指导价格,由价格部门负责,最初是计委,2003 年改组为发改委,2018 年国家医保局成立,药品和医 疗服务价格也归其管理;从管理形式上来看,逐步规范、逐渐放松,从最初的严格政府定价,至改革开放允许 少数项目按成本定价,后续实行非盈利机构政府指导价。但医疗服务价格长期偏低,仍需进行调整。2016 年 7 月 1 日,国家发改委、卫计委、人社部、财政部发布《推进医疗服务价格改革意见》,要求进一步缩小政府定价 范围,逐步理顺医疗服务比价关系,目前公立医院也有部分特殊需求、个性化需求医疗项目可以进行市场定价。 配合取消药品加成,全国大部分公立医院已经相应调整了部分医疗服务价格;随着全面取消耗材加成,医疗机 构需要再次调整医疗服务价格,预计未来 2-3 年将迎来各地医疗服务价格的集中调整,全国统一的医疗服务项 目技术规范也有望出台。腾笼换鸟,已有多地探索医疗服务价格的优化。2018-2019 年,深圳、北京、浙江等多地探索取消耗材加成, 同时调整医疗服务价格。对比浙江、北京、深圳三地的医疗服务价格调整,我们发现三地均涉及取消耗材加成、降低检验价格、提高人工服务价格。我们认为医改将持续深化调整医院盈利模式和行为模式,在医疗服务收入 占比继续提升的同时,价值回归服务本质。长期看,医疗服务价格调整有望进一步规范医生处方行为,对刚需 的药品、耗材有利,也有利于民营医疗、体检产业等医疗服务行业的长期健康发展。医保:支付方式改革,长期引导医疗资源合理配置中长期看,DRGS 将成为影响住院支出最重要的政策之一。DRGS 将于 2020 年开始在 30 个试点城市模拟 测算、2021 年实际付费,这种医保结算方式适用于绝大部分住院患者。从美国的经验看,DRGs 对行业整体影 响有限,但是结构性影响明显,尤其对住院支出增速影响较为显著。CHS-DRG 分组与付费技术规范出台,医保局顶层设计基本完成。2019 年 6 月 5 日,医保局、财政厅、卫 健委、中医药局发布《关于印发按疾病诊断相关分组付费国家试点城市名单的通知》,确定了 30 个城市作为 DRG 付费国家试点城市,主要任务如下:①实行按 DRG 付费还需两年。按照“顶层设计、模拟测试、实际付费”三步 走的思路,确保完成各阶段的工作任务,确保 2020 年模拟运行,2021 年启动实际付费;②健全 DRG 付费的信 息系统。统一使用国家制定的疾病诊断、手术操作、药品、医用耗材和医疗服务项目编码的基础上,完善医保 付费信息系统;③统一 ADRG,各地自行制定 DRGs 分组。在核心 DRG(A-DRG)的基础上,根据当地实际,制 定地方 DRG 分组体系和费率权重测算等技术标准,实现医保支付使用的 ADRG 分组框架全国基本统一。2019 年 10 月 24 日,国家医保局发布《国家医疗保障 DRG 分组与付费技术规范》和《国家医疗保障 DRG(CHS-DRG) 分组方案》,标志着顶层设计基本完成。DRGs 结算适用于绝大部分住院患者。根据医保局《技术规范》,CHS-DRG 适用于急性住院病例(占绝大 部分住院病人);不适用情况包括:①门诊病例;②康复病例;③需要长期住院的病例;④某些诊断相同,治疗 方式相同,但资源消耗和治疗结果变异巨大病例(如精神类疾病)。统一的技术规范和分组方案。此次医保 DRG 分组的原则有四点:①逐层细化、大类概括;②疾病诊断、手 术或操作临床过程相似,资源消耗相近;③临床经验与数据验证相结合;④兼顾医保支付的管理要求和医疗服 务的实际需要。从具体分组来看,国家统一的 ADRG 以临床经验和临床路径为主,各地分组的细分 DRGs 则是 以统计分析为主。……创新药:关键词是“国际化、差异化、效率及开放融合”政策催化和结构调整,重磅肿瘤新药大放异彩,真正进入产品为王的时代行业关键词是“效率、国际化、差异化及开放融合”大型创新药企在中国市场亦面临快速创新转型的压力,效率仍将受到企业高度关注。根据我们统计,2018 年大型创新药企(包括跨国公司)在中国市场的原研药或仿制药收入占比均在 60%以上,2019 年随着创新药的 放量,预计这一比例将会快速降低。考虑到 2020 年开始仿制药集采将会加速,大型创新药企仍会高度重视研发 和商业化效率问题。创新药医保目录谈判机制下,国内创新药定价存压,国际化及差异化能力凸显。2019 年 10 月,医保局启 动新一轮医保谈判,新增 70 个药品,平均降价幅度 60.7%,续约 27 个药品,平均降价幅度 26.4%。其中,三种 丙肝治疗用药降幅在 85%以上。考虑到国内医保控费需求,我们看好具备国际化能力的药企,全球化能力意味 着能够在全球市场分摊高昂的研发费用。为提高效率,开放融合亦成为新药研发领域的一个趋势。从目前行业内的合作模式上看,主要有对其他厂 家品种的 license-in 以及企业间各自药物的合作开发两种模式。我们统计了 2018 年至今 A 股和 H 股主要的创新型公司药物 license-in/out 的情况。近两年复星医药先后引 入了 10 余个创新品种,研发管线已经具备一定规模, 后续有望逐步走向收获期。其他如石药、绿叶等综合性药企以及百济、信达、君实、贝达等 biotech 公司均有各 自的品种引进或合作研发开展。恒瑞医药在 2018 年初先后对其 3 种在研新药进行了海外研发的授权,我们认为 这同时也是国内企业加强海外新药市场布局的一种有效模式。CXO:维持较高景气,不同思路都有好的选择国内转型及国外产业转移将为医药外包行业提供长期机会受益于创新研发升温,行业持续高增长从业绩增长上看,医药外包板块直接受益于目前国内创新药、创新器械的研发热潮,增速持续上升,行业 维持高景气度。由于板块内公司体量分化较大,部分公司财务准则对测算有明显影响,我们剔除了缺乏同比数 据和财务数据波动巨大的公司,2019Q1-3 收入增速为 27.98%,归母后扣非增速均在 50%左右,整体行业增速 相较中报仍有一些提速,并且在 2018 年同期高基数的情况下依旧保持上涨。2018 年以来,医药板块整个板块 持续维持在高增长阶段。行业订单充沛,高景气度预计持续。从近年医药外包主流公司的在手订单来看依旧保持在高增长的水平, 且全行业在持续进行产能扩张,景气度较高。泰格医药 2018 年新增订单 33.08 亿,待执行订单 36.83 亿,增速 均在 30%以上。博济医药 2018 年新增订单 4.3 亿,待执行订单累计有 8.3 亿。昭衍新药在手订单约为 8 亿,同 比增长 19.40%。合全药业披露 2018 年底在手订单为 27.2 亿元,2017 年同期为 3.4 亿美元,也实现了较快的增 长。龙头公司员工人数、人均产值持续向上当前国内外包企业的员工人数、人均产值和国际龙头相比还有较大差距,同时国内的外包企业享有中国工 程师红利和成本优势,随着全球的产业转移,未来提升空间较大。2018 年底 CRO 龙头药明康德、康龙化成、泰格医药、昭衍新药等员工人数仍在持续上升,同时伴随着人 均创造收入、利润的上升。反映出龙头公司的公司规模体量仍在快速扩大,而且收入、利润的增速高于员工数 量增长。CMO 公司中龙头公司合全、凯莱英员工数量及创收也均保持上升,药明生物由于新建产能,员工人数大幅度提升,在业绩高增速下人均创造利润也同步实现了快速上涨。相继公布股权激励,维持员工稳定由于 2018 年以来行业的持续高景气度,当前国内医药外包行业的人员流动性较高,伴随而来的是人员成本 的相应提高。因此医药外包企业相继推出股权激励政策,维持公司员工稳定性的同时,同时进一步提升员工积 极性。而从股权激励的解锁条件上看,部分公司的高要求体现除了业绩高增长的信心,同时也反应当前行业的 高增长。2020 年外包行业评估,行业景气度持续整体估值比较:高景气度对应高估值参考现在行业龙头 CRO、CMO 公司的估值水平和增速预测,我们认为当前行业估值仍处于相对合理的水平,泰格医药、药明康德、 昭衍新药、康龙化成为代表的 CRO 企业对应 2020 年约 50 倍左右 PE,小分子 CDMO 代表企业凯莱英在 40 倍 PE 左右,药明生物在 75 倍 PE 左右。同时,根据当前的盈利预测增速,代表性医药外 包公司对应 2021 年的估值水平基本符合 PEG 为 1 的状态。对比 90 年代海外 CRO 行业的估值水平,我们认为 这是当前行业高景气度状态下对于业绩确定性高的行业的合理估值溢价。维持较高估值中枢的前提是行业仍处于高景气状态,反应到实际各家公司,各个细分赛道有不同的细分景 气度指标,通过评估各个领域的最新进展和行业趋势,我们认为整体来看 2020 年医药外包的高景气度状态仍将 持续。药物发现:新技术平台应用热度升温,新药研发多样化增强药物发现作为整个研发流程的最前端,企业对于产品本身的靶点、质量等的关注点是放在首位的。而当前 研发成功率的降低更增加了药物发现阶段的重要性。2018 年,国内以 DNA 编码化合物库、PROTAC 技术、ADC 药物平台、双抗研发平台、细胞治疗研发平台等技术平台或方法的关注度持续提升,同时也提示了国内药物的 研发从小分子领域延伸到单抗、双抗、ADC、细胞治疗以及核酸药物的趋势正在不断加快。龙头公司对于新技术平台的扩展和应用进度较快,订单获取情况良好。药明康德 DNA 编码化合物库分子数 量超过 800 亿个,拥有 6000 多个自己合成的骨架分子,目前仍在持续扩大中。而国内 DEL 的龙头企业成都先 导也即将登陆科创板。康龙化成、美迪西也均在拓展自身的 DEL 业务。生物药方面,药明生物的双抗平台推出 后订单获取情况良好,迅速和国内外龙头企业建立了多项合作关系。同时随着技术的成熟,CAR-T、ADC 等领 域也逐渐增加了众多平台型企业。我们认为从源头来看,药物种类的不断拓展将持续推动外包行业的增长。临床前 CRO:细分龙头产能持续扩建昭衍新药 2018 年太仓的新动物顺利投入使用,产能增加近 70%,同时先后决定在重庆、广州分别投资 7.87 亿、11 亿建立新的安评中心,以服务于不同地区的制药企业。同时药明康德也在苏州扩建了自己的安评中心, 持续扩大自己的产能。泰格的控股子公司方达医药也快速扩建了自己在上海、美国的生物分析实验室,并扩大 自己在国内的 CMC、安全性评价业务。我们认为行业的龙头公司快速的产能扩张提示临床前业务目前仍处于高增长的阶段,以昭衍新药为代表的 细分领域龙头需求程度高,在手订单充分,预计新产能投入后能够快速提升使用效率,推动业绩的增长。而以 药明康德、康龙化成为代表的综合型企业订单具备一定持续性,前期药物发现业务的快速增长对后续业务有引 流作用,有望通过一体化平台带动临床前试验业务的增长。临床 CRO:临床试验登记数量维持较高水平临床试验成本成为当前龙头公司研发费用的主要投入项目。以恒瑞医药医药为例,公司 2018 年在临床试验 设计和临床试验的直接投入(物耗、材料等)上的投入最多,分别为 6.08 亿元和 4.70 亿元,占总研发投入的 39.27%和28.10%,且两个项目增速均在50%以上。在人员人工上,公司投入增长35.20%,占总研发投入的18.45%。 恒瑞的研发体系建设较为完善,人力成本提升相对较小,分析复星、贝达、君实的数据,可以看到除了在临床 试验及技术服务上有较大支出和增长,三家公司在人力成本上的投入占比和增长也相当高。从上述数据可以看出,临床试验、技术服务或是第三方外包的费用基本占据各大公司研发支出的首位。而 临床试验支出的增长主要来自于重要品种的 II、III 期临床试验或是海外的临床试验开展。以肿瘤为代表的临床试验登记数目仍在持续快速增长。从行业整体水平来分析,以肿瘤这一目前国内药物 研发最火热的领域为例,根据 CDE 药物临床试验登记与信息公示平台的数据和 2018 年中国肿瘤临床试验蓝皮 书统计,2018 年国内的各期临床试验数目相较 2017 年均有明显提升,I 期临床增长最多。由于临床试验持续时间往往超过 1 年,目前反应的研发投入上的增长可能是 2017 年甚至之前开展的临床试 验投入。根据这个趋势,考虑到一定比例的 I 期试验成功后企业将进一步开展后续研发,而且 II、III 期临床试 验投入相较 I 期试验有明显增大,我们预计未来研发费用高增长仍是行业中优质企业的普遍趋势。国内研发龙头临床试验维持高增长。我们分析了代表性企业近几年肿瘤领域开展临床试验的数量。以恒瑞、 百济等有重磅品种处于临床后期或者迫近上市的企业近两年开展临床数目显著增多,当然后续的研发管线储备 也是重要影响因素之一。从试验开展数目上可以看到一定的未来研发费用趋势,同样是考虑到临床试验的持续 时间问题,我们预计行业中龙头公司的研发投入仍将有快速的提升。临床 CRO 的收入增速的前瞻指标可以参考 IND 的登记情况、临床试验登记情况、临床试验成本等因素。 根据 CDE 的登记数据,2018 年 CDE 临床试验登记中心共登记 2968 项临床试验(由于 2018 年起增加了 ChiCTR 文号的预实验、上市后试验等,数量有所增多),2019 年截至 12 月 10 日共登记了 2878 项临床试验。评估其中 不同阶段的临床试验,BE 试验数量 2019 年相较 2018 年有一定下滑,而 I 期、II 期、III 期试验数量基本维持一 致。由于临床试验持续时间较长,对于临床 CRO 而言,基本为分阶段收取费用。我们认为临床试验数量的提升 对于行业景气度的影响仍会持续。需求端的提升也带来临床试验费用不断攀升。由于①临床试验趋于复杂化、②监管要求不断提高、③临床 试验中心数量不足费用提升、④从业人员需求提高薪资增长等原因,当前临床试验成本仍处于不断上升阶段。 我们认为国内当前的临床试验方面的高需求、成本提升一定程度上也将维持临床 CRO 的收入提升,行业高景气 度有望持续。CDMO:订单延续性高,早期订单高增长国内以凯莱英、合全药业、药明生物为代表的 CDMO 企业均已经形成了漏斗型的订单结构,博腾股份、九 洲药业等也正在加强前端研发能力。我们认为几个驱动因素提示 2020 年 CDMO 行业仍将维持较好增长:①2019 年大部分 CDMO 企业早期临床订单数量增长迅速,在有良好的订单延续性的前提下,会带动后续收入增加;② CDMO 行业往往需要提前为下一年的订单排期和布局,而当前龙头企业的订单排期情况良好;③不同开发阶段 的药物均有 CDMO 需求,临床试验、上市产品数的增多均提示 CDMO 需求的增长。此外我们认为全球 CDMO 行业向以中国为代表的亚洲地区转移的趋势仍在持续,且国内 CDMO 的业务覆 盖正从中间体向原料药和制剂进行下游拓展,将继续带动 CDMO 的订单保持较快增长。仿制药产业链:寡头垄断大势已定,积极关注上游痛点试点落地,扩面在即,大格局已定仿制药价格体系重塑大势所趋已经完成的两轮国家集采产品降幅明显,第三轮即将启动。2018 年 12 月和 2019 年 9 月,国家先后进行了 两轮集采,从竞标结果来看,25 个品种在两轮竞标中的平均降幅分别达到了 54%和 25%,部分竞争较为激烈的 品种降幅达到 80-90%,而且集采的覆盖区域也从最初“4+7”的 11 个试点城市扩大到全国。2019 年 12 月 1 日, 第三轮集采前的企业座谈会在上海召开,确定了基本的方案和品种,预计即将启动。集采药品价格接近全球底线,龙头的商业模式注定是产品组合及一体化优势集采后,国内药品销售、制造成本优势造就全球低价。我们统计了 4+7 和第二轮集采招标的 25 个品种的全 球价格情况,对比美国、日本、印度的价格,集采招标之后的药品价格基本已经接近全球主要药品市场中的底 线价格。我们认为,未来仿制药龙头的商业模式注定是产品组合及一体化优势,单品种价格已不那么重要。仿制药产业链投资:积极关注上游痛点关注行业痛点,高标准原辅包需求增大一致性评价关联审批加强原辅包企业市场选择权。2017 年 12 月,国家药监局发布了《原料药、药用辅料 及药包材与药品制剂共同审评审批管理办法》的征求意见稿,结合 MAH 制度,明确建立了以药品上市许可持 有人为责任主体的药品质量管理体系,以药品制剂质量为核心,原辅包为质量基础,原辅包与制剂共同审评审 批的管理模式。而一致性评价要求下,原料药、辅料、包材和药品将进行关联审批,意味着一旦原料药、辅料 或者包材进行更换,药品需要重新进行申请,更换成本相较原来有明显的提升。在这种条件下,原辅包企业在 供给端的话语权相较会有所提升。带量采购后制剂销售壁垒下降,原辅包企业下游拓展能力提升。国内仿制药行业的传统销售模式下,销售 能力较强的企业往往能够获得更大的市场份额,而带量采购的推广使这一局面发生了转变。参与集采的品种一 旦中标后会获得承诺的使用量,对于销售端的压力有显著降低,同时意味着新进入市场的企业面临的销售壁垒 显著降低,有利于原辅包等上游企业对于下游制剂产业链的拓展。原料药:环保压力带来产业结构性升级,原料药、制剂一体化企业占优环保压力促使原料药行业进行结构性升级,产品质量、生产工艺提升。2012 年以来,国家先后发布多项环 保政策,针对污水、废水、大气污染等进行了限制。医药制造企业相应的环保支出有较为明显的提升,众多产 能面临环保整治和退出的压力,行业集中度持续提升。而相应的龙头型原料药企业的生产质量、工业改良、污 染处理能力也有了提升,实现了产业上的结构升级。原料药、制剂一体化企业在成本控制上占优,产品增量明显。对于本身拥有原料药、制剂生产供应的企业 企业而言,一方面原料药的供应上可以更为稳定,另一方面在原料药的生产成本控制上也更具优势,加上后续 制剂销售壁垒的下降,后续的成长动力较强。建议关注华海药业、仙琚制药、科伦药业、普洛药业等。辅料:行业集中度低,国内公司规模较小国内对于辅料的重视程度长期不足,一致性评价和新型制剂研究带动辅料行业提升。国内目前正在使用的 辅料大约有 540 种,药典收纳的辅料标准约为 270 个,而美国、欧洲正在使用的辅料品种数量为 1500、3000 种, 药典收录的分别有 750、1500 种,我国使用的辅料品种显著落后。而当前一致性评价政策、以及对于新型制剂 开发的关注度提升使国内辅料的重视度得到提升。国内辅料行业的集中度较低,代表性公司规模相对较小。我国专业化的药用辅料生产企业不多,一些常规 辅料多由化工、食品生产企业生产。而药品审批的关联审评有望带动辅料行业产业提升,新型、高端辅料的开 发和应用速度有望加强。建议关注 A 股的代表性企业为山河药辅等。包材:受益于注射剂一致性评价一致性评价要求产品包材不低于原研。2019 年 10 月 15 日,国家药监局发布了《化学药品注射剂仿制药质 量和疗效一致性评价技术要求(征求意见稿)》。相对于 2017 年的版本,本次公布的征求意见稿中对于直接接触 药品包材的要求从“不建议使用低硼硅玻璃和钠钙玻璃”更改为“注射剂使用的包装材料和容器的质量和性能不 得低于参比制剂”,同时承认了美国、欧洲、日本的包材标准。国产药用玻璃瓶替代升级将加速,市场需求带动价格、集中度提升。而当前国内主要的药用玻璃瓶仍以低 硼硅玻璃和钠钙玻璃为主,相较海外药企主要使用中性硼硅玻璃和钠钙玻璃。在一致性评价包材不低于原研药 的要求下,国内的低硼硅玻璃将持续向中性硼硅玻璃升级,产品替代将加速。而中性硼硅玻璃的生产难度较大, 大部分国产企业与海外公司产品质量尚有一定差距,虽然国内产品价格较低,但是受市场认可的公司较少,受 技术壁垒影响,后续市场集中度和竞价格局有望持续提升。建议关注具备技术和生产优势的内药用玻璃龙头山 东药玻。政策波动下,寻找布局早、有品种群、有增量的企业长期看,我们对仿制药格局变化推演没有变:阵痛难免,遵循“布局早、品种群及有增量”的主线自下而上 寻找受益标的。整体而言,我们认为仿制药集中采购的镇痛难免,寻找相对确定的受益品种可以遵循布局早、 品种群及有增量几条主线,建议积极关注华海药业、科伦药业及中国生物制药等。疫苗:强监管、批签发逐步正常化,重磅品种价值凸显强监管背景下,重磅品种价值凸显2019 年 12 月 1 日,《中华人民共和国疫苗管理法》正式实施,从严格行业准入、提高处罚力度、加强安全 生产等措施强化了行业的强监管力度。在此背景下,重磅品种价值进一步凸显。疫苗批签发机构即将迎来扩容,批签发速度有望迎来提升批签发机构数量有限,叠加疫苗事件导致批签发速度趋缓。现阶段,我国进行批签发机构中检院可独立签 发全部疫苗品种;七个省所负责指定区域内企业疫苗产品的无菌及异常毒性等指定项目检验,并将结果报送中 检院;上海所除可进行指定项目检验外,可独立签发指定区域内批签发申请人申报的流感疫苗。叠加“长生生物” 疫苗事件,2019 年批签发速度趋缓,10 月以来批签发速度已有小幅恢复。《省级疫苗批签发机构授权方案》出台在即,疫苗批签发机构数量有望迎来扩容,批签发速度有望提升。 根据第十九届生物制品年会公布信息,《方案》有望在 2021 年底前完成现有现承担血液制品批签发、目前也同 时承担疫苗批签发部分检查项目的省所疫苗批签发机构授权,最终逐步建立与我国疫苗产业和监管需求相适应 的国家疫苗批签发机构网络体系。截至目前已在部分地区开展了部分疫苗品种的批签发培训,将于 2020-2021 年进行相应的评估考核并结合批签发工作需要进行遴选授权实现批签发机构扩容。综合考虑检验方法难易程度、检验任务轻重差异等情况,优先推动流感、水痘、流脑、Sabin—IPV、乙肝、乙脑、甲肝、百白破、狂犬病疫 苗等的批签发实验室建设工作。批签发数据跟踪:批签发速度回升,行业整体降幅缩窄,7 大品类实现增长1-11 月,批签发速度略有提升,累计批签发量同比下滑 1%,降幅较 1-10 月继续缩窄,品种整体格局稳定。 2019 年 1-11 月,疫苗行业整体批签发量为 48849 万支,同比下滑 1%,下滑幅度较 1-10 月继续缩窄,主要受长 生生物疫苗事件及疫苗法出台监管趋严导致批签发速度下降影响,现阶段批签发速度已有提升,未来批签发机 构有望扩容,批签发速度有望继续提升。2011-2018 年,行业整体批签发量由 79402.9 万支下降到 54076.3 万支, CAGR 为-4.7%。……连锁药店:行业逻辑逐步兑现,龙头公司仍存较大发展空间我国零售药店行业规模稳健增长,连锁化率持续提升根据米内网数据:1)2019 年上半年我国零售药店终端药品销售额实现 2098 亿元,同比增长 7.4%,增速较 2018 年企稳,维持快于全终端合计增速的趋势;2)零售药店终端市场份额 2019 上半年占比为 23.1%,较 2018 年底提升 0.2 个百分点。根据《中国药店》统计数据,近十年我国药品零售行业集中度持续提升:1)CR10 市 场份额由 2010 年的 11.52%提升至 2018 年的 21.58%;2)连锁药店数量由 2008 年的 12.9 万家提高到 2018 年的 25.5 万家;3)连锁化率由 2008 年的 35.4%提高到 2018 年的 52.2%。我们认为,随着未来药品价格体系的逐步调整、行业监管趋严、医保账户资质的逐步调整,未来零售药店 行业会进一步加强与工业企业的合作,中小连锁及单体药店经营承压推动行业集中度持续提升,头部连锁企业 在行业变革过程中将率先受益。政策推动行业向规范化前行,集中度进一步提升2018 年下半年以来,零售药店行业相关政策变化较大,整体来看国家层面及地方层面的政策在推动行业向 规范化前行,集中度的进一步提升及处方外流进程的提速:1)打击骗保:2018 年全国共检查定点医疗机构和零售药店 19.7 万家,查处违法违规定点医药机构 6.6 万 家,医保资金安全是医保控费的重要一环,未来随着打击骗保行动的常态化,行业竞争将逐步趋于良性,龙头 公司有望率先受益;2)药店分类分级管理:a)药店分类分级的最终结果是行业向规范化前行,将淘汰经营不规范中小连锁及 单体药店,带来集中度提升;b)医保定点药店向高等级药店倾斜,同时高等级药店有望率先获得门诊慢、特病 统筹医保资质,率先推动门诊慢、特病药品的处方外流,加速我国处方外流整体进程;c)实行网上集中审方的 连锁药店企业三类门店可视为配有 1 名执业药师,减少了连锁药店企业的执业药师数量需求,降低了连锁药店 企业的经营负担;3)整治执业药师“挂证”:整治工作将有力打击药品零售行业违法违规现象,尤其中小连锁及单体药店考虑 经营成本往往是不规范现象的重灾区,本次整治工作将进一步加大中小连锁及单体药店经营压力,有望加快行 业集中度的提升速度;4)集采扩围:短期零售渠道价格面临逐步调整,但是长期来看国家鼓励医保定点药店自愿使用省级药品采 购平台进行国家集采品种的采购,可以从价格及品种双维度解决部分集采处方药采购难题,头部连锁企业医保 店占比维持在 70%-80%的水平,在集采调整过程中有望率先受益;5)网售处方药解禁:新版药品管理法未直接禁止网售处方药,标志着多年以来网售处方药禁令的解除。从 政府监管、民众用药常识普及程度、民众用药安全及支付手段等角度综合考虑,未来网售处方药大概率采取有 条件逐步放开。与西方发达国家相比我国药店密度较高,为 O2O 模式提供了很好的网点布局,相比邮寄模式优 势明显,也符合国家倡导的“网订店取”或“网订店送”的药品新零售方式。我们静待网售处方药细则的出台,迎 接线上线下相互赋能融合,共迎行业发展;6)广东省处方外流体系逐步完善,改革示范效应明显:a)采购端,今年 9 月,广东省药店处方药纳入省 级采购平台,在价格及品种双维度解决了此前部分处方药采购难题;b)销售端,广东省于 2018 年 4 月推行省 内药店分类分级管理,高等级药店可实现全品类经营,12 月发文完成慢病统筹支付资质在药店的落地,龙头公 司将率先受益;c)广东省是我国改革排头兵,已经走出推进医药分开探索处方外流的相对完善体系,示范效应 明显,未来随着全国版分类分级管理办法的逐步推行,全国范围内推动零售药店提供慢病用药服务有望成为可 能医保个人账户政策推演:加强共济属性,扩大门诊统筹,开展大病医保筹资端:国家标准,各地微调,账户划拨比例已在弱化。城镇职工基本医疗保险基金筹资主要由用人单位 缴纳的基本医疗保险费、职工个人缴纳的基本医疗保险费、基本医疗保险费的利息、基本医疗保险费的滞纳金、 依法纳入基本医疗保险基金的其它资金共五部分构成。职工用人单位和个人共同缴纳的基本医疗保险费为城镇 职工基本医疗保险基金主要收入来源。现阶段用人单位缴费划拨账户已根据当地基本情况进行相应调整,同时 部分地区单位缴费并未按照 30%的比例全部划拨个人账户,而是划拨给门诊统筹及个人账户。城镇职工个人账户资金使用效率较低,当年结余已达千亿元并逐年攀升,累计结余 2018 年底突破 7000 亿 元。支出端:城镇职工个人账户探索多元化支出路径,加强共济功能。个人账户支出占城镇职工医保支出比例 约 40%,其中药店为个人账户支出的主要部分,支出占比达 39%。现阶段,多地个人账户已开始探索多元化支 出路径,加强共济功能,其中包括购买商业医疗保险、家庭共济使用、门诊支付及住院支付等。个人账户未来演化方向之一:加强共济属性。由于城镇职工基本医疗保险个人账户制度运行过程中出现的 种种问题,在我国各个地方实践中,已经开始对个人账户制度进行了改革,以不断地盘活个人账户,扩大个人 账户的使用功能。主要改革方向是个人账户受益人范围不断扩大(主要形式为家庭共济),使用功能不断增多(可 用于购买商业健康保险,保健食品,个人体检、疫苗等各种与个人健康相关的项目)。个人账户未来演化方向之二:门诊统筹。 1)我国城镇职工医保制度中,职工的门诊保障主要依靠个人账户。 在开展门诊统筹的问题上阻力较大,问题也相对复杂。在全国范围内开展的地区相对较少,而且主要集中在经 济发达地区。从目前公开报道的情况来看只有广东省和葫卢岛、泰州、镇江、连云港、厦门、温州、秦皇岛、 呼和浩特、南京、金华、上海、淄博、杭州、宁波、成都、青岛等城市对职工医保门诊统筹制度进行了不同程 度的探索,总体上仍处于试点阶段;2)其筹资方式主要分两种,一是从个人账户或应划入个人账户的基金中划 转一部分,二是从统筹基金结余中划拨。采取第一种方式的代表性城市有青岛、淄博,其在保留个人账户的同 时,通过基金划转建立起了职工医保门诊统筹。其他城市则利用统筹基金结余建立起门诊统筹,并不同程度地 拓宽了个人账户的使用范围。外部环境变化带来板块投资机会:药店龙头争夺统筹机会医疗渠道,一方面国家全面推动带量采购,在品种结构、处方来源等多角度推动处方外流;另一方面,卫 健委已发文全面叫停药房托管,17 省发文探索剥离门诊药房,进一步加速处方外流进程。现阶段,行业监管趋严、医保政策小幅收紧,推动行业向规范化前行,头部企业合规经营率先受益,中小 连锁及单体药店经营压力凸显,未来行业集中度提升仍将持续。城镇职工医保个人账户改进工作是整体医改工程中的重要一环,预计城镇职工医保个人账户仍将保留,存 量资金继续留存的同时可能加强共济属性,增量资金逐步削弱,改进工作对医药零售行业直接影响有限。最新版《药店分类分级管理指导意见》,明确指出医保管理部门优先选择高评级药店签订医保服务协议,纳 入定点药店范围。鼓励通过高评级药店提供门诊特殊病、门诊慢性病用药的医保费用结算服务;我们认为:1)长期来看,门诊统筹资质与个人账户有望完成平稳交接过渡,门诊统筹资质将为药品零售行 业带来增量客流及增量市场,推动行业持续健康发展;2)零售药店行业头部企业的全国布局仍在持续,未来将 继续享受政策红利,在个人医保账户改进及药店分类分级管理的进程中更多的承接门诊慢、特病药品零售业务; 3)随着网售处方药的有条件放开及国家倡导 O2O 业务模式,线上线下将进一步融合实现双向赋能;4)线下药 店作为终端借口,将依托交互体验的特点加速新业态探索为客流提供更多增值服务,推动行业健康发展。重点 推荐益丰药房、老百姓、大参林、一心堂(排名不分先后)。医疗器械:进口替代仍是最大的投资主线,大小公司均有机会医疗器械进口替代逻辑:市场+技术+政策“市场+技术+政策”三因素共振促进进口替代拐点来临。从市场来看,我国医疗器械行业增速远超全球医 疗器械行业,未来十年将成长为全球医疗器械大市场;从技术来看,全球范围多个医疗器械领域技术已发展较 为成熟,国内产品正在快速追赶进口产品,同时工程师红利和完善的配套产业链政策,为国内生产企业提供良 好的成本和竞争优势;从政策角度来看,分级诊疗、鼓励进口替代、取消药品和耗材加成等政策促使医院采购 更重视高性价比的国产器械。国产医疗器械迎来快速发展的黄金时代。全球范围来看,大市场培育大企业,中国具备培育出全球医疗器械市场的环境和空间。目前全球医疗器械 行业前二十大医疗器械企业主要分布在欧洲、美国和日本,其中原因之一是欧洲、美国和日本在全球医疗器械 市场中的占比分别为接近 40%、30%和 10%。我国医疗器械市场增速为 15-20%,远超全球 5%左右的增速,有 望在 10 年后占据全球 25%的市场份额。广阔的本土市场也为本土企业提供了良好的成长空间。从全球医疗器械行业技术发展历程来看,多项器械领域已达技术平台期。19 世纪以前医疗器械行业技术主要为简单的治疗和诊断技术,19 世纪到 1950 年左右第二次工业革命推动了多项医疗器械技术的发展,70-80 年 代电子医疗器械浪潮推动了 CT、核磁等技术迅速发展,90 年代以后新材料和计算机技术的发展也带动了医疗 器械领域的创新和信息化发展。近年来多项医疗器械技术已进入技术平台期,外企产品主要为升级和改进为主, 突破性发明或创新技术较少,国内企业正在快速追赶。工程师红利和配套产业链完善,为我国医疗器械企业的研发生产优势提供了重要基础。以迈瑞为例,电子 元器件、电路板、芯片、模具等多大多数医疗器械零配件均可在国内采购,对外采的依赖度逐渐降低,我国相 关器械供应链完善和工程师红利成为国产器械高性价比的重要基础。各细分领域:关键技术突破推动产品力提升,部分品类仍有较大改善空间在医学影像设备领域,彩超、内窥镜等器械正处于快速替代期。医学影像设备中,市场空间较大的为核磁、 CT、彩超、DR 等,目前国内产业链较为完善的 DR、生命监护、彩超等品类已与进口产品性能比肩,但高端 CT 和核磁共振尚有十年的技术代差。目前监护仪和 DR 已占据大部分市场份额,彩超、软式内窥镜、硬式内窥镜等器械正处于快速替代期。在心血管介入领域,部分产品已实现进口替代,部分产品与外企并跑或领跑。目前金属心脏支架已实现进 口替代,微创医疗的支架已经可以挑战全球支架金标准;可降解支架领先外企在国内应用,正在快速放量; 左心耳封堵器和 TAVR 等领域,国内企业和国外企业几乎同步创新和发展,并根据亚洲人心脏结构进行了多项 创新和改进。其中经导管介入瓣膜领域的长期市场空间有望追赶心脏支架。骨科部分品类已实现进口替代,人工关节正在加速追赶。脊柱和创伤领域国产化率已经较高,随着近年来 爱康、春立、威高等国产品牌人工关节的设计和技术快速追赶,高端产品线逐步丰富,近年来龙头公司出现业 绩加速的情况,外企的增速和份额有减小趋势,国产化率持续提升。部分医学影像领域核心零配件自产化能力提升、心脏支架和骨科领域产品力提升,是进口替代的关键因素。 在医学影像设备领域中,监护、彩超、内窥镜等设备的绝大部分零配件均可在国内采购到,DR、CT、核磁的高 端零配件主要依赖进口。心脏支架和骨科的部分核心原材料依赖进口,原材料厂商也是全球各大企业的供应厂 商,所以对产品性能提升和进口替代不形成限制因素。医疗设备:看好在等级医院有高竞争力的企业进口替代机会巨大,看好在等级医院产品有竞争力的企业。医疗设备销售终端主要为等级医院、基层市场 及民营医院,我们预计基层及民营医疗市场增速将有放缓,但是新品周期+进口替代放量的企业,业绩仍有望维 持高增长。由于不同品类在不同终端分布差异较大,以彩超为例,公立等级医院销售占比在 60%以上,我们长 期看好以迈瑞和开立为代表的国产彩超龙头在等级医院的进口替代机会。1) 分级诊疗:已有政策利好逐渐减小(持续到 2020 年),未来需观望有无新的政策出现乡镇卫生院和社区卫生服务中心:2019 年前实现达标建设;县级医院:第一阶段提升 500 家县级医院综合能力(2014-2017 年),第二阶段全面提升 1000 家县级医 院综合能力(2018-2020 年)。2)鼓励进口替代政策持续推进:16 年、17 年开始多地政策落地,利好国产龙头;产品达到高端替代水平 的企业,业绩维持高速增长(如迈瑞)3)民营市场(民营医院+体检机构)短期来看增速放缓,长期来看空间较大。民营医院市场对医疗设备的 采购近年来维持 13-15%的高增长,但是 19 年民营医院受医保核查影响较大,预计 20 年影响减弱。高值耗材:招采政策变化,小而美的细分龙头仍然有成长机会高值耗材招采政策是市场关注焦点。考虑到高值耗材的分类管理、质量评价、使用习惯及物流配送等多个 环节的特征,我们认为在 2-3 年的时间窗口内,该领域的集采仍然会以省级招采为主。招采体系的逐步规范化 和上收,有利于细分龙头市场份额提升,长期我们仍然强调创新是最重要的投资要素。主要政策进展如下:1)耗材加成:2019 年底前取消耗材加成2)两票制:全国范围内有 25 省已开始实施耗材两票制,预计 2020 年更多省份两票制方案会出台。3)耗材治理:国家发文要求 11 个医改试点省份加快复制推广三明经验,江苏、安徽已经执行了省级高值 耗材带量采购,山东、辽宁、山西、海南、云南、广东等省份已经发布省级带量采购实施方案或明确表明要开 始执行高值耗材带量采购,大多尚未确定集采品种。国家医保局已明确重点治理目标为临床用量大、采购金额高、临床使用成熟、多家企业生产的耗材,并在 2019 年底前由国家卫健委和国家医保局负责完成第一批重点治理耗材名单。与药品相比,医用耗材的复杂程度 更高,例如耗材没有通用名,品种规格繁多、市场分散,耗材使用人员的水平直接影响医疗效果等。我们预计 各地集采将首先从容易标准化、品种规格少的品种入手,对于大部分市场规模尚小、未形成充分竞争的细分领 域,短期内不会开展国家层面集采。下一步,医保局将选取重点品种实施“带量采购”的试点工作;建立全国医用耗材监控平台,实现全国范围 内数据共享;为创新型医疗器械顺利挂网销售扫除障碍。国家卫生健康委将配合相关管理部门建立耗材一致性 评价机构。短期来看,耗材带量采购以地方试点为主,目前全国多地已开展或计划开展带量采购试点。宁波规则为较 为成功的耗材采购模式之一,2016年宁波以全市公立医院耗材采购量为筹码,对五大类耗材进行价格谈判降价, 其中骨科脊柱类和人工关节类降价幅度最高,整体来看性价比较高的国产耗材占比提升。2019 年以来,江苏、 安徽等地也开展了带量采购工作,京津冀、湖南、山西、宁夏、海南等地已发布工作意见或实施方案,大多尚 未发布采购品种及具体方案。已实施带量采购的品种中,大多数品种平均降幅为 50%左右。各地已经进行带量采购的品种涉及心脏支架、 起搏器、人工晶体、关节、脊柱、创伤及低值耗材等多个品类,其中部分国产化率高、扣率较低的骨科品种及 部分低值耗材品种降幅较高,目前人工晶体、起搏器等国产化率较低的品种降幅较低。国产 IVD 行业:政策影响暂远,高景气细分领域稳健增长体外诊断作为临床诊疗的重要辅助工具,一直以来持续快速增长,2018 年预计市场规模超过 700 亿元,增 速预计在 15-20%之间。从细分领域来看,以化学发光技术为核心的免疫诊断、以肿瘤靶向药物伴随诊断为主要应用的分子诊断、以及床旁快速诊断 POCT,是 IVD 板块中市场空间大、国产公司最有投资机会的细分市场。 此外检验自动化流水线的国产化趋势已基本确立,国产公司中安图、迈瑞、迈克等先后发布国产流水线产品, 预计将迅速成为国产 IVD 行业新的业绩增长点。体外诊断产品临床应用具有特殊性,短期看大范围集采不具备可操作性当前市场较为关心体外诊断产品的集中采购问题,我们认为短期暂不具备可操作性。首先,体外诊断产品 本身应用较为特殊,除血球仪、血凝仪、尿液分析仪、及少量 POCT 试纸条类检测产品外,通常需要在检验仪 器和诊断试剂的配合下来完成对待检标本生理生化指标的检测。其次,如将体外诊断产品集中采购,需要考虑 或解决三个方面的问题:1)仪器种类较多,且各家检验参数上通常会有差异,因而不是标准化产品,在检验质 量一致性评价未完成前,单独考虑价格因素会导致技术降级;2)检验试剂种类则更加繁多,且部分试剂为特定 型号仪器的专用试剂,通常医院在安装机器完成后,再更改其他品牌会造成仪器浪费,且厂家或经销商也通常 在商业采购协议上有采购时间约束; 3)检验试剂一直以来都是医院采购的成本项,试剂价格经过多年招标竞价, 相对于检验服务收费价格扣率已处于较低位置。因此,体外诊断实行像药品一样的带量采购政策难度较大,短 期不具备可操作性。当前各地方检验服务收费价格陆续调整,2019 年以年初深圳及年中北京价格调整较为典型。深圳作为计划 单列市,医疗服务收费价格自主定价,新方案更多是在原来方案上价格调整,检验服务整体降价 10%,涉及到 人工的检查和医疗服务普遍涨价。北京医疗服务收费改革则具有重大指导意义,北京是在执行 2012 年发改委颁 布的《全国医疗服务价格目录规范》,2019 年 6 月执行后,有望起到示范性作用,有利于全国各省和计划单列 市逐步出台新一版医疗服务收费方案,从医疗服务项目名称和编号上实现统一,有利于将来全国实施 DRGS、 电子病历等重要医疗改革。北京医改方案中检验价格基本稳定、整体有利于国产进口替代。检验项目价格分项目来看,生化和免疫项 目与现行北京收费价格相比,基本保持稳定,只有个别项目降价;同时北京此前使用进口和国产试剂的收费差 异此次调整中被拉平,使用国产试剂的价格有明显提升,这将有利于实现进口替代。分子诊断项目取消此前的 按方法学收费,实行按检测项目收费,更加科学严谨,对于现有主要检测项目如 EGFR 基因检测,由于检测位 点极多,价格应能保持相对稳定。另一方面,由于诊断试剂进医院价格已经处于较低扣率,检验收费价格的相 对稳定也有利于 IVD 产品进医院价格的合理稳定。化学发光是 IVD 诊断进口替代最大细分市场化学发光正逐步取代酶联免疫,行业增速近两年预计超过 20%,我们预计 2018 年市场规模为 260 亿元(出 厂端口径)。化学发光目前已形成“4+5”竞争格局:进口品牌为主,罗氏、雅培、贝克曼、西门子四家合计占比 超过 80%;国产五大家新产业、安图、迈瑞、迈克、亚辉龙,2018 年合计占比预计在 12%,合计收入在 30 亿 元左右。假设未来 3-5 年国产化学发光诊断市场规模增长至 300 亿元(考虑招标降价因素),假设国产公司占据 50%市场份额,市场规模可达到 150 亿元,进口替代有 5 倍空间。国内化学发光诊断企业近年来取得长足发展,从仪器性能角度看,新的国产化学发光设备参数已与进口品 牌不相上下。从国内竞争格局看,按 2018 年发光业务规模排序:新产业、安图、迈瑞、迈克、深圳亚辉龙,其 他国产厂家销售额不超过 1 亿,较有竞争力的厂家包括厦门万泰、苏州长光华医、江苏泽成等。长期来看,由 于迈瑞和安图当前继续保持 50%以上的高增长,国产厂家中未来迈瑞和安图大概率占据前两位。国产化学发光进口替代的难点主要在于:1)仪器性能;2)试剂配套完整度、或检验菜单 丰富度;3)与自动化流水线产品的协同销售。检验流水线作为 IVD 集大成者,市场前景广阔从各项技术的发展历程来看,自动化都是各项检验技术共同的发展趋势。生化、免疫、微生物、分子诊断、 血球诊断领域都已实现全自动检测,全自动生化仪、全自动化学发光免疫分析仪、全自动血球仪等产品已非常 成熟,而一条全自动的实验室流水线系统将各个模块连接,实现样本处理、传送、分析、数据处理的全自动化 操作,具有多方面优势,是目前临床诊断技术的最高水平。国内具备安装条件的医院预计不少于 2000 家,其中部分三甲医院不止 1 条,我们简单测算流水线装备需求 医院家数和流水线装配量,预期未来总装配数可能超过 3000 条。目前国内已安装近 1500 条,主要为进口品牌 (罗氏、雅培、贝克曼、西门子),国产厂家中安图生物已实现装机,迈瑞、迈克、新 产业、亚辉龙、科华等国产厂家也已于近期发布。国内企业开始冲击流水线新装市场,对国产厂家而言,我们认为实现大规模装机的难点主要在两个方面: 1) 流水线产品被临床接受的前提是检测模块需要具有优异的性能,对国产品牌而言,高速生化仪和化学发光仪是 其中重要组件,生化仪和化学发光仪性能好坏是临床决定是否采用的重要考量。2)目前国产流水线体的研发和 生产目前尚未国产化,进口采配成本较高,整体成本相较于进口并未有明显优势,主要是国产销售政策较为灵 活,可以先从二甲或小三级医院入手。POCT 诊断向高精度低成本方向发展POCT 是从生化、免疫、分子等诊断领域分化出来的领域,技术转化相对容易,随着各块市场的高速增长, 除已上市的万孚生物、基蛋生物外,有 POCT 业务或正在进入这块业务的上市公司越来越多,免疫荧光和小型 化学发光技术已逐渐成为市场主流。国内 POCT 快速诊断 2018 年预计市场规模超过 40 亿元(不含血糖检测), 进口品牌较少,主要是美艾利尔、罗氏、生物梅里埃等,国产厂家中如万孚、基蛋等营收快速增长。国产 POCT 厂家经过多年技术积累,已实现 POCT 免疫胶体金向免疫荧光技术的升级,目前小型化的 POCT 化学发光正开始推广。对国产厂家而言,进口替代的难点在于技术,智能化、小型化的 POCT 仪器将更符合国 内临床诊断要求,我们预计 POCT 市场国产占有率预计为 50%左右,未来更多是国产品牌之间的市场竞争和行 业洗牌。分子诊断市场更重视仪器国产化,肿瘤伴随诊断高景气我国分子诊断市场规模较小,但增长迅速,按出厂口径计算,2016 年市场规模预计超过 100 亿元,增速超 过 20%。分子诊断产品和服务端以国产厂家为主,进口品牌主要是罗氏、梅里埃等。从细分市场景气度来看, 受益于肿瘤靶向药纳入医保及降价、以及大量肿瘤新药上市,作为创新药产业链的伴随诊断市场持续保持高增 长,上市公司中从 PCR 产品向 NGS 产品扩展的艾德生物充分受益。基因测序是基因检测行业的金标准,综合优势明显,是未来分子诊断的主流方向。根据 2001 年人类基因组 计划研究结果,人类基因组有 2.5 万个基因,未来随着基因检测数量和通量的快速增长,基因测序将展现出与 其他分子诊断技术相比明显的综合优势:成本低、高通量、准确性高等。但与 PCR 产品仪器和试剂基本国产化 相比,NGS 产品仪器的国产化程度非常低,主流二代测序市场 80%被 illumina 公司占据,国产公司中仅华大智 造的 BGI 测序仪在小范围使用和销售。由于测序芯片需要和测序仪配套使用,Illumina 一家独大使得 NGS 测序 服务公司的刚性成本居高不下,测序服务行业普遍处于增收不增利状态,因此分子诊断行业仪器的国产化更为 重要。第三方医学检验行业持续稳健增长,已步入投资收获期我国第三方医学检验行业(Independent Clinical Laboratory,ICL)经过近 20 年发展,行业格局已基本稳定, 金域、迪安、艾迪康及达安营收规模居于前列。2018 年 ICL 行业收入规模预计达到 144 亿元,同比增长 21%。 根据卫生统计年鉴,2018 年我国卫生医疗体系检验检查总收入 5800 亿元,ICL 占比仍不到 3%,相对欧美成熟 市场 40%的检验服务占有率,仍有极大提升空间。我们认为连锁第三方医学检验具有两点核心优势,非常符合当前医疗政策:一是连锁后的规模效应带来成 本优势,二是高端检测技术的可及性提高。基于这两点,随着医保控费及分级诊疗政策的不断推进,公立医院 逐渐提升检验服务外包率,ICL 行业长期增长动力强劲。第三方检验行业两家上市公司表现靓丽,龙头金域医 学股价涨幅超过 150%,主要动力在于行业龙头均已布局完成,逐步进入业绩兑现期。血制品行业:长期供给收缩价格企稳,底部弱复苏血制品行业 2019 年整体表现良好,我们认为其主要原因是供给端的收缩,行业采浆增速在 2016 年达到高 点后,2019 年持续下滑至个位数。2018 年全国采浆约 8600 吨,仅增长约 7%,这使得今年上半年国产血制品供 给偏紧,同时进口白蛋白批签发在 2019 年上半年同比亦出现下滑,使得行业渠道库存快速下降,价格从今年一 季度起触底回升。长期看,由于全国新批浆站仍较少,成熟浆站的采浆增长不快、甚至部分浆站由于献浆员年龄结构老化等 问题,当前采浆政策下,整体采浆增速预计仍将保持低位,这将有利于血制品价格保持稳定或温和上涨,有利 于血制品行业集中度提升,龙头公司采浆增速高于行业将使得业绩保持稳定快速增长。2020 年投资策略:破旧立新,结构性投资 2.0 版2019 年回顾:围绕产业新格局,优势赛道与核心资产表现优异2019 年:科创板拓展投资视野,新的估值体系在快速形成中医药生物是科创板热门行业,投资者视野进一步向更早期公司拓展,新估值体系亦在快速形成中。截至 12 月 18 日,共有 186 家企业申报科创板,其中医药生物相关的共有 40 家,占比 21.5%,医药生物是科创板的热 门领域。从细分行业看,40 家生物企业中有 20 家属于医疗器械行业,9 家属于生物制剂行业,8 家属于化学制 剂行业,3 家属于 CRO 行业。其中,泽璟制药、百奥泰、天智航、前沿生物、神州细胞、君实生物等 6 家公司 选择标准五上市,使得投资人视野进一步向更早期公司拓展,基于管线价值评估的 DCF 体系亦在快速形成中。2020 年:破旧立新,结构性投资的 2.0 版展望 2020 年,我们看好医药行业的结构性投资机会 2.0 版。行业格局变化势不可挡,与即将过去的 2019 年相比,明年医药投资不变的是继续深化产业思维,破旧立新,精选优势赛道。我们看好创新药、CXO、仿制 药产业链上游、疫苗、医疗器械、医疗信息化、连锁医疗及药房等赛道。明年发生变化的是投资可能向纵深发 展,我们建议坚定持有核心资产,同时积极关注具备性价比优势的细分龙头。(报告来源:中信建设证券)(获取报告请百度搜索“未来智库”,登录下载。)
 慎到
慎到南科大生物医学统计中心揭牌,要创建一流的数据分析实验室
南都讯 记者朱倩10月23日下午,南方科技大学生物医学统计中心揭牌。该中心将集中在复杂性数据分析(包含精准医疗和公众健康研究)、适应性临床试验和数据分析、统计组学数据分析(包含生物学、高效计算技术)等方向的研究,并与南方科技大学医学院、生物系、化学系、深圳应用数学中心,南方科大医院,深圳市儿童医院等科研机构和院系建立紧密联系,联合开展生物医学领域的研究,创建一流的数据分析实验室。该生物医学统计中心旨在建成具有国内一流水平和国际影响力,集基础研究,多学科交叉融合,咨询,专业人才培养以及产业转化为一体的综合科研基地。【来源:南方都市报】声明:转载此文是出于传递更多信息之目的。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 邮箱地址:newmedia@xxcb.cn
 天与地
天与地赵超代表:用计算医学填补生物医药领域的“短板”
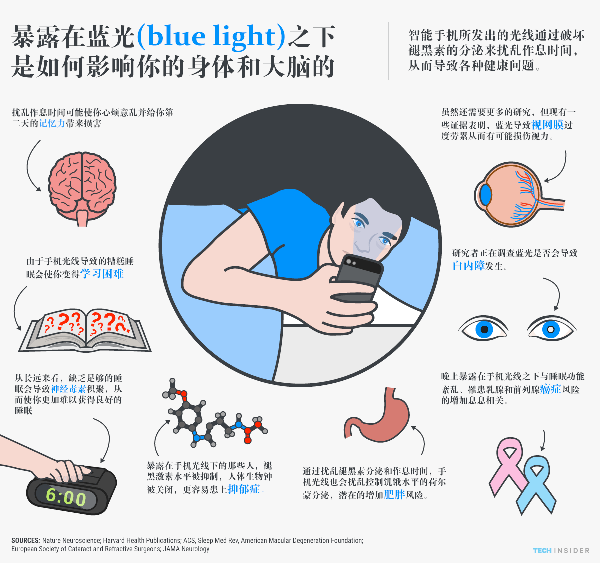
“我国需要进一步加快布局计算医学新型数字基础设施,发挥算力、人工智能方法、大数据作为使能技术的带动作用,充分释放生物医学大数据的价值,赋能我国医疗和制药产业。”今年两会,全国人大代表、步长制药总裁赵超带来了一份关于布局计算医学新型数字基础设施的建议。当前,全球生物医药领域正处于底层技术迅猛变革的转型期。以基因治疗、肿瘤免疫学等为代表的生物医学技术和以人工智能、大数据为核心的信息技术形成了双轮驱动力量。计算医学正是以信息科学与生物医学交叉融合为基础,深度挖掘生物医学大数据获得全新医疗价值。“它能够提供全新药靶,加速新药研发,提升慢性病与疑难症医疗水平,大幅减轻患者用药负担,全面提高医保基金使用效率,同时为后工业革命时代产业发展以及社会进步提供全新发展方向。”赵超说。据了解,目前基于人工智能的新药研发平均1~2年就可以完成临床前药物研发,全世界利用该技术的在研药物管线约200个。预计到2028年,人工智能为生物医药行业每年可节省约700亿美元的研发成本。从全球范围来看,人工智能、大数据在生物医药的应用虽然还处于早期阶段,但全球诸多知名制药企业都纷纷与人工智能企业进行研发合作。“我国生物医药产业正处在由仿制向创新迈进的关键爬坡期,仅依靠传统制药技术难以实现产业超越,这就需要数据技术和制药技术双轮驱动。”赵超表示,这将为我们“补短板、创未来”赢得极佳的时间窗口。不过,当前我国生物医药产业智能化升级还存在诸多制约因素。赵超表示,虽然生物医学数据已经进入了PB级时代,但是从计算医学角度看, 95%以上的现有数据只能满足统计学意义的回顾性研究。数据碎片化、标准多样化、数据库建设低水平重复,个体数据不够立体,共享机制不足等问题较为突出,数据难以有效融合处理。比如,在药物临床试验通常投入大、耗时长、失败率高,而计算医学可以发挥空间很大。但由于行业界限,临床领域与计算医学协同创新积极性不高,影响新药研发的成功率和产业价值的提升。另外,对人工智能、大数据的认知不足也是不可回避的问题。一项对全球超过300位药物研发科学家的调查显示,41%的被调研者并不了解人工智能技术“这就更谈不上如何让他们利用机器学习、知识图谱等技术进行新药开发。”赵超表示,这种认知不足会导致关键决策者对新技术产生主观的不信任,进而导致不敢也不愿意对新的数字基础设施做出投入决策。基于此,赵超提出加快布局计算医学新型数字基础设施的政策建议。他认为,应由科研力量国家队牵头,推动“计算医学”新型数字基础设施建设。依托在国内学科深度融合方面布局早,发展好的科研单位,比如中科院计算所、中科院基因组所、哈尔滨工业大学等单位牵头建设计算医学的共性技术平台。采访中,记者了解到,国内一些单位通过计算医学技术发现了当前主要应用于激素受体阳性Her2阴性乳腺癌患者群体的热点药物CDK4/6抑制剂的新临床场景,如果通过临床试验取得成功,将会给药企带来百亿美元利益。赵超建议,应由国家相关部门对计算医学的共性技术平台的建设给与一定的政策资金支持,用于扩容数据中心等硬件基础投入和学科交叉团队的培养。通过集约化建设,避免重复投资、重复建设带来的资金浪费与时间窗口流失的问题。其实,早在2016年,美国食品药品监督管理局血液和肿瘤产品办公室(OHOP)就与美国卫生和人类服务部在肿瘤学领域启动了一项跨学科创新计划——信息交换和数据转换计划(简称“INFORMED”计划)。该计划旨在利用大数据和高级分析技术的力量来服务于精准药物开发,包括探索新的研究终点,药物靶标和患者分组策略等。赵超还建议,由国家药监局与国家卫健委、科技部联合牵头启动计算医学虚拟联合实验室,打破深度交叉的界别限制,组建跨学科的专家咨询委员会,协助生物医药企业、医疗机构梳理可适合数据驱动的业务场景。另外,上述实验室还可以定期举办跨学科的交流沟通会,增强两大学科领域的相互理解。通过该机制引导相关企业、机构克服对新一代信息技术认知不足的瓶颈,打破应用障碍,向大纵深推进到药企,助力医药研发做出精准、客观的投入决策。此外,完善生物医学大数据的数据标准,推动有条件开放共享,保障数据要素质量,促进数据要素规范化流通也是必经之路。“以先进的计算技术补上生物医药领域的短板,利用计算医学新基建布局未来,相信我国生物医药产业一定会实现‘弯道超车’。”赵超说。
 人见其歧
人见其歧人类微生物组研究设计、样本采集和生物信息分析指南
人类微生物组研究设计、样本采集和生物信息分析指南A guide to human microbiome research: study design, sample collection, and bioinformatics analysisChinese Medical Journal [IF: 1.585]DOI: https://doi.org/10.1097/CM9.0000000000000871Review: 2020-6-26钱旭波1, 陈同2, 徐益萍1, 陈雷3, 孙馥香4, 卢美萍1, 刘永鑫5,6浙江大学医学院附属儿童医院风湿、免疫和变态反应科中国中医科学院中药资源中心首都医科大学附属复兴医院易汉博基因科技(北京)有限公司中国科学院遗传与发育生物学研究所中国科学院大学,生物互作卓越创新中心钱旭波和陈同为共同第一作者通讯作者:卢美萍,浙江大学医学院附属儿童医院风湿、免疫和变态反应科,中国浙江杭州竹竿巷57号,邮编:310003,邮箱:meipinglu@zju.e.cn摘要这篇综述的目的是为医学研究人员,特别是那些没有生物信息学背景的研究者提供简单易懂的微生物组学知识,包括研究中常用的概念、技术和分析方法等。首先,我们介绍了基本概念,例如微生物群(microbiota)、微生物组(microbiome)和宏基因组(metagenome)等。然后,我们讨论了研究设计方案、样本量计算方法以及提高研究可靠性的方法。我们特别强调了阳性和阴性对照的重要性。接下来,我们讨论了微生物组研究中常用的统计分析方法,重点关注多重比较的问题以及组间β多样性分析的方法。最后,我们介绍了生物信息学分析的具体流程。总之,严谨的研究设计是获得有意义结果的关键步骤,而适当的统计方法对于准确解释微生物组数据很重要。通过阅读这篇文章,研究者能获得研究设计、样本采集和生物信息分析等全方位的微生物组学知识。关键词:微生物组、研究设计、统计分析、样本量、生物信息分析、分析流程1. 前言随着测序技术和数据分析方法的发展,近几年医学微生物组研究领域出现了一些令人瞩目的成果[1-3],比如微生物组与代谢性疾病[4-6]、消化系统疾病[7-10]和心血管系统疾病[11]之间的关系日益明确。这些发展和发现增加了医生在微生物组研究方面的兴趣,进而也涌现出了大量有价值的论文[12]。另外,随着QIIME 2[13]和多组学方法[1, 9]等先进技术和分析流程的出现,微生物组分析方法也不断进步。然而,理解和掌握这些技术和分析流程并非易事,特别对于医生来说更是如此。本文的目的是为研究者,特别是那些没有生物信息学背景的医生提供易懂的微生物组学知识,这些知识包括详细的微生物组学基本概念、科研设计方法、样本采集和保存方法、统计分析方法以及生物信息分析方法。我们希望医生们通过阅读此文能够快速掌握以上知识和方法,进而有效地挖掘数据背后的生物学意义。2. 基本概念2.1 Microbiota、Microbiome等术语Microbiota(微生物群/微生物组)是指定植在人体特定部位的微生物,包括细菌、古菌、病毒、真菌和原生动物[14, 15]。在医学研究中,如果测序技术采用的是16S rRNA基因(又称为rDNA),则microbiota是指细菌和古菌。Microbiome是指整个微生境,包括微生物、基因组和周围环境[14, 15]。不过,microbiota和microbiome有时存在混用情况。我们建议,如果你的研究仅涉及微生物本身,则应该使用microbiota,否则应该使用microbiome(图1)。例如,如果研究者想探索肠道短链脂肪酸与微生物的关系,使用microbiome更合适。宏基因组(metagenome)是指微生物基因组的集合[14],一般用鸟枪法宏基因组测序获得,宏基因组学则是研究宏基因组的学科[12, 14]。病毒组(virome)指人体内或表面的病毒集合,包括内源性逆转录病毒、真核生物病毒和噬菌体[16]。研究病毒组的学科就是病毒组学。作者注:Microbiota国内有些学者翻译为“微生物群”,microbiome翻译为“微生物组”。不过中文文献用“微生物组”或“××菌群”即可,多数情况下不需要区分是microbiota或microbiome。图1:微生物组、微生物群、宏基因组和16S rDNA的概念。(A)微生物组(microbiome)的概念不仅涵盖微生物,而且涵盖周围的环境条件。微生物群(microbiota)仅指微生物本身。(B)宏基因组是指微生物的所有基因组,而16S rDNA仅涵盖基因组的一部分。(C)α多样性衡量样本中的多样性,而β多样性比较样本之间的物种差异。2.2 细菌层级分类细菌分类最常用的层级为门、纲、目、科、属、种、株。例如,临床上十分常见的大肠埃希菌的层级分类见表1。表 1: 大肠埃希菌细菌层级分类2.3 操作分类单元和扩增子序列变异操作分类单元(operational taxonomic units,OTUs)的构建对于标记基因(扩增子)数据分析非常重要[17]。OTU是指一组高度相似的序列,通常将具有97%相似性的一组序列归为一个OTU[18, 19]。不过,这种OTU的方法有显著的缺点,它人为地设置一个相似性阈值,漏掉了细微的和真正的生物学序列差异[20]。最近开发的扩增子序列变异(amplicon sequence variants, ASVs)方法可以解决这些问题,它使用序列变异信息将序列数据解析为准确的序列特征。ASV具有单核苷酸分辨率,并且具有比OTU相似或更好的敏感性和特异性[20]。注意,OTU或ASV不等于物种,一个OTU / ASV可能包括多个物种,反之亦然[21]。2.4 α-多样性α-多样性是指样本内的多样性,常见的样本有粪便,唾液或支气管肺泡灌洗液等[15]。医学研究中经常使用3种α多样性指数:Chao 1指数、香农指数和辛普森指数。Chao 1指数主要反映物种数量(richness),它计算时考虑以下三个因素:物种数量、单条序列数量和双条序列数量[22]。这意味着它不能反映微生物组的丰度(abundance)。香农指数结合了丰度和均匀度信息[23],它赋予稀有物种更多的权重[22],这意味着当稀有物种的数量增加时,它的值会更大。香农指数的值通常不超过5.0;它的值越高,α多样性就越丰富[22]。辛普森指数也整合了丰度和均匀度,不过与香农指数比较,计算时它对常见物种有更大权重。它的值介于0-1之间,这个值越大,α多样性越丰富[22]。在以上指数中,richness是指一个样本中物种的数量[17, 24],而abundance(丰度)指物种的原始序列读数[24]。如果原始序列读数被转换成百分比后,它就称为相对丰度。2.5 β-多样性β-多样性是指样本或组间的微生物组差异,通常用于了解两组微生物组组成的差异是否显著。在这里,我们关注两个常用的β多样性指数:Bray-Curtis相异性和UniFrac距离。Bray-Curtis相异性是一种用于量化两个样本或组间的物种组成差异的指标,其值的范围是0到1,其中0表示两个样本或组间具有相同物种,而1则表示它们不共享任何物种[25]。此外,它在计算时给予常见物种更大的权重[23]。请注意,Bray-Curtis相异性不是真正的距离度量指标,因此用“Bray-Curtis相异性”的叫法比“Bray-Curtis距离”更恰当[22]。UniFrac距离可以不加权,也可以加权,它基于系统发育距离估算微生物组样本或组间的差异[26]。未加权的UniFrac距离只考虑了物种是否存在,它对于检测稀有物种的数量变化很敏感,但是在计算中忽略了丰度信息[27]。加权UniFrac距离计算时纳入了丰度信息[28],并减少了稀有物种的权重[29]。2.6 排序排序用于探索数据结构,由降维后的正交轴图形表示。排序图是可视化β多样性的有效方法。排序可以分为2大类:非约束排序和约束排序[30-32]。如果图形上的点不受环境因素(样本元数据)的约束,这种排序叫做非约束排序,否则叫约束排序[32]。常用的非约束标准包括主成分分析(principal component analysis, PCA)、对应分析(correspondence analysis, CA)、主坐标分析(principal coordinate analysis, PCoA)和非度量多维标度(non-metric multidimensional scaling, NMDS)[30, 32]。常用的约束排序有冗余分析(rendancy analysis, RDA)和典范对应分析(canonical correspondence analysis, CCA)[31, 32]。微生物组信息是高维数据。PCA通过将数据以几何方式投影到较少的维度上来简化复杂性,它在计算中使用欧几里得(Euclidean)距离[30]。通常情况下它并不适用于物种丰度数据的分析,因为PCA分析的数据必须是线性的[30]。但是如果物种数据经过Hellinger转换,则PCA可以用于物种数据分析[30]。相反,CA适合于物种丰度数据分析,而且无需预先转换数据。在CA分析中,所有样本均使用Pearson卡方距离进行排序[30]。但是请注意,稀有物种可能会对CA分析产生过大影响[33]。如果研究人员希望基于相异性指标来对样本或特征进行排序,那么PCoA是一个不错的选择。在微生物组研究中,PCoA分析最常使用Bray-Curtis相异性和UniFrac距离。NMDS用于表示排序图中样本的相对位置。与PCoA相似,NMDS分析可以使用任何距离或相异矩阵。参考文献[30]详细介绍了PCoA和NMDS之间的差异,在大多数情况下PCoA比较常用。RDA是一种结合了PCA和回归的约束排序,它的响应矩阵是微生物组数据,解释矩阵是临床指标(样本元数据)。RDA对于显示微生物组数据是否受临床指标影响很有用。但是请注意,由于PCA计算过程要求响应矩阵的数据结构必须是线性的,因此可能需要对数据进行预转换。最后,CCA其实就是CA的约束版本,它具有CA的基本特性和缺点[31]。3. 研究设计3.1 研究设计方案严谨的研究设计对于获得准确而有意义的结果很重要。医学微生物组研究中最常使用的研究方法包括横断面研究、病例对照研究、纵向研究和随机对照试验(randomized controlled trial, RCT)。前3种是不应用干预因素的观察性研究,而最后一个是典型的实验性研究。横断面研究分为描述性横断面研究和分析性横断面研究[34]。前者仅是描述性的,主要用于调查一个或多个人群中的微生物组成,而后者则用于探讨微生物组与健康结果之间的关联。但是,微生物组与健康结果之间的关联可能源于混杂因素,例如性别[35]、年龄[36]、体重指数(body mass index, BMI)[37]、饮食[5, 38]、季节[39]和药物治疗[40, 41]。此外,横断面研究时,微生物组和结果是同时测量的,因此很难确定它们之间的因果关系。通常,横断面研究仅用于探索微生物组的基本特征,并且可以作为后续研究的初步实验。在大多数情况下,微生物组被视为暴露(exposure),疾病被视为结局(outcome)。在这些假设下,传统的病例对照研究很少用于微生物组研究,因为以前的暴露(微生物组)信息很难获得。但是,如果暴露和结局对调,则可以使用病例对照研究设计方案。同样,在上述假设下进行前瞻性队列研究也很困难,因为很难知道哪些微生物是潜在的暴露。而且,定义可用作暴露或非暴露因素的特定微生物组并非易事,因此难以将研究对象确定为暴露或非暴露个体。在实践中,有或没有疾病的个体通常归入研究组或对照组,然后在不同时间点前瞻性地收集含有微生物组的样本[17]。也就是说,前瞻性队列研究中的研究对象通常根据临床结局而不是特定的微生物组模式进行分组。RCT或其他实验研究的目的是评估干预措施的有效性。干预措施可以是药物或微生物组。例如,粪菌移植研究中的干预措施是微生物群[42, 43]。值得注意的是,对照组的选择应恰当。以上这些研究设计中应注意匹配混杂因素,这部分内容将在下面讨论。有时对照的选择很困难,尤其是在临床研究中干预措施是微生物群本身的情况下。在这种情况下,如果其他研究设计不合适,那么进行有对照组的前后自身对照试验(controlled before-after trial)或历史对照试验将是一个不错的选择[44]。3.2 定义纳入和排除标准定义确切的纳入标准和排除标准可以使组间更好地匹配,并且有利于控制混淆因素,比如年龄[36, 45]、性别[35]、BMI[46]、饮食[47]、季节因素[39]、药物治疗[40, 41]、种族[48]、地理区域[45]和共存疾病等[7]。年龄可显著影响微生物组,对于那些小于16岁的人更是如此[36, 45]。因此,对于涉及儿童的研究,年龄必须很好地匹配。饮食是另一个对微生物组改变有影响的因素,所以也要进行匹配[47]。为了增加组间的可比性,地理区域因素在研究设计时也需要考虑在内[45]。由于药物治疗对于微生物组有显著影响,所以入组前数月内接受过药物治疗的患者应该排除在外[41, 49],这里讲的数月通常指入组前3~6个月[49]。3.3 微生物组研究的样本量和检验效能计算在进行研究设计时估计样本量大小非常重要。适当的样本量可使微生物组研究识别出组间的差异,并节省资源和时间。但是,样本量和检验效能计算对于研究者来说仍然是一个挑战[50]。微生物组研究中最常用的样本量和效能计算方法可以用t检验、方差分析、χ2检验和Dirichlet多项式模型[51]。以t检验为例,分3个步骤确定样本大小和效能计算。首先,通过初步实验获得少量扩增子数据。其次,使用R包vegan计算出每个样品的香农指数[52]。最后一步是使用R软件包pwr中的power.t.test()函数计算样本量和效能。当研究者仅关注两组之间物种多样性的差异时,可使用t检验计算样本量和效能。在参考文献[51]中有样本量和效能计算的详细介绍。3.4 阴性和阳性对照的重要性微生物组研究的结果可能会受到多种因素的影响,例如DNA提取试剂盒、采样方法、污染和测序方法等[53],不过可以通过使用阴性和阳性对照来减少这些影响。不幸的是,以前的研究中只有30%报告使用了阴性对照,只有10%报告使用了阳性对照[53]。使用对照对于准确认识微生物组非常重要,尤其是当样本的微生物含量较低时。以前的研究发现,过去被认为是无菌的标本(例如胎盘和关节液)可能会被微生物定植[54]。但是,这些阳性的结果可能是由其他因素导致的,例如污染。有趣的是,这些低生物含量标本在采用阴性和/或阳性对照后已被证明是无菌的[55]。因此,我们建议当样本为低生物含量样本(例如血液、羊水、脑脊液、关节液和胎盘等)时,应考虑使用阴性和阳性对照。值得注意的是,阴性对照和阳性对照在病毒学研究中也很重要,因为病毒和细菌通常是同时进行检测的[16]。此外,R包decontam可用于鉴定和去除扩增子和宏基因组学数据中的污染物序列[56]。3.5 测序方法的选择微生物组研究中使用的测序方法包括扩增子测序、宏基因组测序和宏转录组测序。扩增子测序包括适用于细菌和古菌的16S rDNA测序以及适用于真菌的内部转录间隔区(internal transcribed spacer, ITS)测序。每种测序方法的优缺点在这两篇参考文献中有详细讨论[17, 57]。简而言之,扩增子测序很便宜,可应用于受宿主DNA污染的低生物含量标本,但一般仅能注释到“属”层级,并且易受某些固有偏倚来源的影响,例如PCR循环数[58]。宏基因组测序方法对样品中存在的所有DNA进行测序,包括细菌、病毒、真核生物和宿主的DNA。它不仅将其分类学分辨率扩展到“种”或“株”的水平,而且还提供了潜在功能信息[17]。但是,扩增子和宏基因组测序方法都无法区分死微生物或活微生物[17]。转录组测序仅产生群落的活跃功能信息。鉴于这些测序方法的优缺点不同,建议将多种测序方法整合在一起以优化研究设计。简而言之,测序方法的选择主要取决于实验成本和样本质量。扩增子测序通常用于获得微生物群落的概况[59],并且通常适用于大规模研究[6, 60]。如果您有足够的项目资金,并且想要获得菌株水平的分辨率和潜在功能,甚至想要恢复整个基因组,宏基因组测序是一种首选方法[61-65]。3.6 提高研究可靠性的方法简单的横断面研究在微生物组研究中的意义有限。在本小节中我们讨论了提高研究可靠性的方法。首先,首选纵向研究或RCT研究,而不是横断面研究或病例对照研究[17, 66]。其次,应计算样本量[51]。第三,混淆因素应匹配,元数据(即各种临床指标等信息)应仔细收集。第四,应详细定义纳入和排除标准。例如,幼年特发性关节炎有几种亚型,每种亚型可能代表不同的疾病[67]。研究者应确定患者组中是否包括所有亚型。第五,最好考虑使用阴性和/或阳性对照[68]。第六,整合其他组学方法,例如代谢组学、转录组学和蛋白质组学,这对于全面了解微生物群落的结构和功能至关重要[17]。因此,应考虑获取微生物群落代谢物概况和/或其他多组学数据。目前,仅探索微生物群落结构的研究不被视为论证效率强的研究设计[17]。最后,建议在动物模型中验证从临床试验获得的初步结果。表2列出了设计临床微生物组研究需要考虑的因素,图2展示了典型的工作流程。实验研究需要考虑的因素见参考文献[49]。表 2: 临床微生物组研究设计需要考虑的要素核对表RCT:随机对照试验4. 样本类型、保存和储藏4.1 样本类型人类微生物组研究的样本类型包括粪便、结肠灌洗液和腔内刷等(表2)。样本类型的选择取决于感兴趣的研究假设。例如,粪便样本易于收集,可用于大规模和纵向研究。另一方面,活检样本对于探索微生物群与宿主之间的相互作用更有用[69]。注意,在一项研究中应该固定采样位置,因为人体的不同部位定植着不同的微生物群[70, 71]。图2:人类微生物组研究的典型流程。4.2 保存和储藏样品保存和储藏的方法应适合实验方法和样品类型。最通用的方法是直接冷冻样品,它可用于各种测序和实验方法,例如扩增子、宏基因组、转录组测序和代谢组学测定。建议将样品收集后15分钟内保存在-20℃下[72, 73],然后在收集24小时内用干冰转移到-80℃冰箱中储藏。不过样本通常是在家里而不是在医院收集的,在这种情况下可以使用保存液。保存液中保存的样本可以在环境温度下保存一周以上[74]。请注意,样品的保存和储藏方法应一致,以最大程度地减少潜在的混淆因素干扰。5. 微生物组研究中的统计分析方法医学研究者通常熟悉单变量统计方法,例如t检验、方差分析、χ2检验和秩和检验。因此,我们在这里仅讨论与多重比较和其他多元统计方法有关的问题。我们首先讨论多重比较会遇到的问题及其解决方案,包括P值调整和使用错误发现率(FDR)。然后,我们讨论其他多元统计方法,例如置换多元方差分析(permutational multivariate analysis of variance, PERMANOVA)和Mantel检验。5.1 多重比较的问题及解决方法由于微生物组数据是高维的,因此多重比较经常在微生物组研究中使用。例如,特征表(feature table)具有成百上千个OTU或ASV,并且每个OTU或ASV都可以进行多次比较。医学研究者经常遇到的另一个例子可能更容易理解。假设一项研究分为3组,例如A组、B组和C组,而研究者想比较这3组之间的差异。在这种情况下就应调整P值,因为每个组都进行了2次比较,即A组与B组,A组与C组,B组与C组。如果有任何组或变量需要进行多次比较则必须进行P值调整,以便减少假阳性率[75]。调整P值的经典方法是控制family-wise错误率,即Ⅰ类错误或α水平。Bonferroni是校正α水平最常用的方法。校正P值的计算非常容易:单个检验的α值除以检验次数。因此,对于上述具有3个检验次数的例子,调整后的P值为0.05 / 3 = 0.017,即只有P <0.017的检验结果才被认为是有意义的[75]。请注意,Bonferroni校正仅适用于多重比较次数较少的假设检验,否则会导致较高的假阴性率(图3)[75]。解决多重比较问题的另一种方法是控制错误发现率(false discovery rate, FDR),它是I类错误或假阳性的数量与所有被拒绝的无效假设的预期比例。例如,如果100个阳性假设检验结果中有5个是错误发现,则FDR为5%。在微生物组研究中,通常使用“Benjamini-Hochberg(BH)校正的P值”而不是原始P值。校正后的P = 原始P * m/i,其中m是检验次数,i是每个P值从小到大排序的序号[75]。如果校正后的P值小于你选择的所选FDR,则认为该检验是有统计学意义的。与Bonferroni方法相比,BH方法不那么保守(即校正强度不是很大),BH法通常用于微生物组特征的多重比较。Bonferroni和BH是最常用的P值校正方法[76],这两种P值校正方法的校正强度见图3所示。图3:不同P值校正方法的校正强度该图显示,Benjamini-Hochberg校正强度小于Bonferroni。随着原始P值的增加,Bonferroni校正法生成的校正后P值快速接近1.0。5.2 PERMANOVA检验有几种统计方法或模型可以用于组间β多样性比较,比如PERMANOVA、Mantel检验、相似性分析(ANOSIM)和多响应置换程序(multi-response permutation proceres, MRPP)。PERMANOVA最常用,并且被认为是以上检验方法中检验效能最大的一种[77],它可通过R包vegan中的函数adonis()实现[52]。vegan包可计算4种常用相异性或距离度量:Bray-Curtis相异性、Jaccard距离以及加权和未加权UniFrac距离[29]。如果PERMANOVA检验的P值小于0.05,则表明不同组间的β多样性差异具有统计学意义;该检验的另一个输出结果是R2,它表示总方差可以用分组因素来解释的比例[29]。5.3 Mantel检验Mantel检验通常用于分析元数据矩阵和微生物组矩阵之间的关联[77],它可使用R包vegan中的mantel()函数实现[52, 77]。该检验的输出至少2个主要统计量:P值和r。与其他类型的相关系数类似,r的值范围是-1 ~ +1[29]。例如,假设研究人员想知道元数据种的分组因素(例如吸烟状态)是否对肠道微生物组的组成产生影响。如果P<0.05并且r>0,这表明吸烟组和不吸烟组之间肠道微生物组的组成不同,元数据矩阵和微生物组矩阵呈正相关。6. 生物信息分析6.1 扩增子数据分析:从原始数据到物种分类表有几种流行的软件或分析流程(pipeline)可用于扩增子数据分析,例如QIIME 2[13]、USEARCH[78]、VSEARCH[79]和mothur[80]。前两者具有许多优点,并已被许多研究者使用和推荐。每种软件或分析流程的优缺点已在我们先前的论文中详细描述[81]遗传:微生物组数据分析方法与应用 和 Protein Cell:扩增子和宏基因组数据分析实用指南。扩增子分析的主要步骤见图4A。我们通常从fastq格式的原始双端Illumina数据开始,最终输出是一个特征表,也称为OTU表或ASV表。第一步是从原始数据中恢复纯净的扩增子序列,因为原始数据包括人造序列产物(artifact),例如引物和标签(barcode)。它包括3个主要过程:合并双端序列,通过标签拆分序列和去除引物。由于原始数据没有统一的标准格式,因此我们需要设计适合上述过程的分析流程。另外,我们也可以使用基因测序公司提供的纯净扩增子数据。图4B显示了用于恢复纯净扩增子序列的典型分析流程。第二步是滤除低质量序列,以便减少背景“噪音”。第三步是识别非冗余序列并且计数。高质量序列仍然有许多人造序列产物,例如错误序列和嵌合体。非冗余序列的计数是找出可靠序列的关键信息。第四步是选择代表性序列(特征)。此步骤基于唯一序列,并通过将序列聚类成OTU或降噪生成ASV来实现[18, 82]。此步骤还包括de novo检测和去除嵌合体。第五步是有参嵌合体检测,这是可选项[83]。通过将序列比对到数据库中,例如rRNA数据库SILVA[84],可以进一步过滤特征序列。应当指出的是,该步骤可以降低假阳性率但易于导致假阴性结果。最后,通过将纯净的扩增子数据与特征序列进行比较来生成特征表(图4A)。然后使用基于RDP[85]、SILVA或Greengenes[86]数据库的分类器实现特征序列的物种分类。此外,基于16S rRNA基因谱,使用PICRUSt[87, 88]、FAPROTAX[87, 89]和BugBase[90]等工具可实现功能预测。6.2 宏基因组分析:从原始数据到物种和功能分类表扩增子测序仅能获得微生物组部分的分类学信息,而且PCR过程很容易产生偏倚和嵌合体[83]。鸟枪宏基因组测序比扩增子测序提供更详细的基因组信息和更高的分类学分辨率[66]。与扩增子方法相比,宏基因组学分析更为复杂,但是它提供了更准确的物种分类、多维度的功能信息,甚至是末培养微生物的基因组草图。宏基因组分析流程如图4C所示。第一步是预处理原始序列数据。原始数据包含低质量的污染序列以及与宿主相关序列。我们可以使用FastQC软件(http://www.bioinformatics.babraham.ac.uk/ projects/fastqc/)进行数据质量检查,然后使用KneadData流程进行质量控制[91]并去除宿主DNA[92]。有关更多KneadData的信息,请访问 http://huttenhower.sph.harvard. e/kneaddata 。第二步是使用基于序列的方法分析物种分类和功能代谢特征。人类微生物组具有高质量的基因集(gene catalog)和基因组[64, 65],因此我们建议使用HUMAnN2[93]工具并采用基于序列的方法进行物种分类和代谢通路分析,该方法高效且易于操作。但是,这种方法只使用一小部分序列信息,而且分析结果受到已知数据库的限制[66]。如果需要发现新物种或基因功能,则需要进行第三步。有几个好的软件工具可以用于将纯净序列组装为重叠群(contigs),例如MEGAHIT[94]和metaSPAdes[95]。然后通过MetaProdigal[96]或Prokka[97]从长序列中预测基因。另外,其他软件工具也可以用于从短序列中预测编码基因,例如MetaGeneAnnotator[98]、MetaGeneMark[99]、Glimmer-MG[100]、MetaGUN[101]、FragGeneScan[102]和Orphelia[103]。为了减少重复基因,在分析多个样品或批次时需要使用CD-HIT构建非冗余基因集[104]。通过采用Bowtie 2[92]或Salmon[105]工具进行比对的方法可以计算基因丰度。目前至少有20个软件工具可用于宏基因组数据物种分类[106]。我们建议使用超快速分类器Kraken 2,它可以提供快速、准确和“种”级别的分类结果[107]。至于功能注释,许多研究人员都推荐使用DIAMOND[108],它是一种快速、敏感的蛋白质比对工具[108]。每个数据库都提供了独特的功能视角,例如,京都基因与基因组百科全书(Kyoto Encyclopedia of Genes and Genomes, KEGG)[109]、EggNOG(一个提供直系同源关系、功能注释和基因进化历史的数据库)[110]、碳水化合物活性酶数据库(Carbohydrate-Active enZYmes Database, CAZy)[111]、致病菌的毒力因子(Virulence Factors of Pathogenic Bacteria, VFDF)[112]和综合抗生素抗性数据库(Comprehensive Antibiotic Resistance Database, CARD)[113]。宏基因组通常包含100~1000个物种[64],很难厘清彼此关系。分箱算法可以恢复无法培养的高丰度菌的基因组草图,并重建系统发育和代谢通路。最后一步是使用metaWRAP[114]或DASTool[115]执行分箱流程(图4C)。这些软件工具有逐步操作教程,并且在其网站上提供了有关人类微生物组的一些样本数据集[81]。另外,几个集成的分析流程,例如MOCAT 2[116]、bioBakery[98]、IMP[117]和微生物组助手(Microbiome Helper)[118],可以执行上述部分或全部分析步骤。你可以在微信公众号“宏基因组”中找到一些受欢迎软件的中文教程。现在你已经获得了物种分类和功能信息文件。通过STAMP或LEfSe可以轻松找到你感兴趣的生物标记[119, 120]。使用R语言或ImageGP(http://www.ehbio.com/ ImageGP)可以将所有结果可视化。图4:人类微生物组研究的生物信息学分析流程(A)扩增子数据分析的主要步骤。(B)扩增子数据预处理的典型流程图:从原始的双端序列到纯净的扩增子。(C)宏基因组测序数据的分析流程。(a)预处理。它涉及删除低质量序列、接头和宿主序列。输出文件是纯净序列。(b)基于序列的分析。它将序列与数据库比对来推断物种分类和代谢特征。(c)基于组装的分析。它将短序列组装为长序列,预测基因,构建非冗余基因集,并与数据库比对进行物种分类和功能注释。(d)分箱。它涉及恢复未培养微生物的基因组草图,并重建系统发育和代谢通路。KEGG:京都基因与基因组百科全书(Kyoto encyclopedia of genes and genomes);eggNOG:基因进化谱系:非监督直系同源群(Evolutionary genealogy of genes: non-supervised orthologous groups);CAZy:碳水化合物活性酶数据库(Carbohydrate-active enzymes database);CARD:抗性基因综合数据库(Comprehensive antibiotic resistance database);VFDB:毒力因子数据库(Virulence factor database)。7. 病毒组在人类疾病中的作用近年来病毒组在人类疾病中的作用吸引了医学研究者的关注[121]。使用病毒组学的方法已发现了许多令人信服的研究成果[122],其中一些技术已经用于临床[123]。在微生物组研究中,病毒组学与其他多组学方法整合后显示出广阔的应用前景。但是,病毒组学研究仍然面临一些挑战。例如,至少40%的病毒序列无法注释[124]。此外,病毒的测序结果容易受到背景噪音的影响[17]。最后,很难获得用于病毒组研究的商业化阳性对照,即病毒模拟群落[16]。8. 总结和结论本文讨论了用于微生物组研究的研究设计、样本收集、统计方法和生物信息学分析方法。在“研究设计”部分,我们强调了研究设计的重要性,特别是设计方案、样本量计算以及用于提高研究可靠性的多种措施。研究设计非常重要,因为不好的研究设计可能会产生无意义的数据。在“统计分析”部分,我们介绍了详细的多重比较P值校正方法。选择合适的统计方法对于准确解释微生物组数据很重要。最后,“生物信息学分析”部分介绍了用于分析微生物组数据分析的方法。本文图中使用的脚本可从 https://github.com/YongxinLiu/Qian2020CMJ 获得。综上所述,对于微生物组研究而言,严谨的研究设计在获得有意义的结果方面具有举足轻重的作用,而适当的统计方法对于准确解释微生物组数据非常重要。循序渐进的分析流程为研究者掌握最新生物信息学分析方法提供了帮助。参考文献略,详见原文Xu-Bo Qian, Tong Chen, Yi-Ping Xu, Lei Chen, Fu-Xiang Sun, Mei-Ping Lu & Yong-Xin Liu. (2020). A guide to human microbiome research: study design, sample collection, and bioinformatics analysis. Chinese Medical Journal Publish Ahead of Print, doi: https://doi.org/10.1097/cm9.0000000000000871相关文章Protein Cell:扩增子和宏基因组数据分析实用指南遗传:微生物组数据分析方法与应用刘永鑫:想学菌群生物信息分析-21分钟带你入门

 40004-98986
40004-98986



